MICROBIOLOGÍA DE ALIMENTOS 4 Y LAS ENTEROBACTERIAS: EL PROBLEMA DE SU RECUENTO EN AGAR VRBG ¿MEJORAR MEDIOS O MEJORAR PARÁMETRO?
MAIL 4 ALIMENTOS: CERTEZA EN TUS RESULTADOS
¿Por qué en el recuento de Enterobacterias, a veces obtengo menor resultado que en el recuento de Coliformes, cuando eso es una incongruencia?
Hoy te invitamos a dejar a un lado los esquemas tradicionales preconcebidos y abrirte a un enfoque diferente: el que funciona. Como dicen los maestros zen: “si quieres tomar un té, vacía tu taza, porque si ya está llena, los nuevos conocimientos no podrán entrar”.
La paradoja del recuento de Enterobacterias: lo que nos enseñan 26 años de experiencia en intercomparación
Tras más de 26 años coordinando el servicio intercomparativo Seilalimentos, hemos aprendido numerosas lecciones curiosas, entre ellas lo que llamamos “la paradoja del recuento de Enterobacterias”.
Dependiendo de la matriz alimentaria y de las cepas utilizadas en el inóculo, muchos laboratorios obtienen resultados inesperados:
* Recuentos más altos de coliformes en VRBL que de Enterobacterias en VRBG
(siendo el mismo medio, en el que sólo cambia la lactosa de los coliformes por la glucosa de las enterobacterias)
* Recuentos más altos de E. coli que de coliformes.
En teoría, esto no debería ocurrir, porque:
* Todos los coliformes son Enterobacterias, pero no todas las Enterobacterias son coliformes. Por lo tanto, debería haber siempre igual o mayor número de Enterobacterias que de coliformes.
* E. coli es el coliforme por excelencia, pero no todos los coliformes son E.coli, por lo que nunca debería aparecer E. coli en mayor número que los coliformes totales.

¿Qué nos dicen estas paradojas?
A quienes llevamos décadas enfrentándonos a este tipo de resultados, lejos de sorprendernos, nos estimulan a buscar las causas y, sobre todo, las soluciones a estas paradojas.
La explicación está en la imperfección de los medios de cultivo (y más aún cuando se emplean métodos indirectos, que siempre son menos robustos que el medio de cultivo). Si los medios fuesen tan fiables como creemos, estas incoherencias simplemente no existirían.
El Agar VRBG, aunque imperfecto, como acabamos de ver, sigue siendo el medio de referencia (y no se ha conseguido mejorar) para un grupo tan amplio, artificial y heterogéneo como son las Enterobacterias —un grupo definido por el ser humano, más que por una realidad biológica, genética o filogenética concreta—.
Innovación para mayor coherencia
En este contexto, en MICROKIT hemos trabajado en alternativas más prácticas y coherentes:
* 1-DryPlates®-ETB:
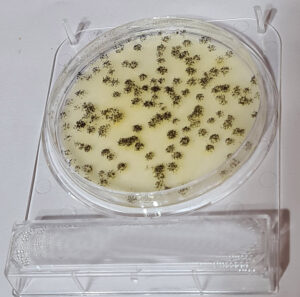
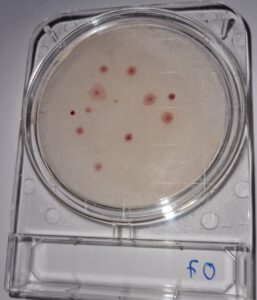
reproducen los resultados del VRBG clásico, pero sin las incomodidades del polvo: la esterilización, la siembra en masa o la doble capa (y en este medio, además, ese olor repugnante a bilis que desprende el polvo).
En apenas 10 segundos de trabajo, se obtienen los mismos resultados, con mayor comodidad y seguridad, y sin tener que respirar un polvo que provoca arcadas.
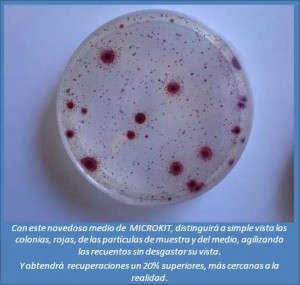
Las placas deshidratadas de MICROKIT ofrecen los recuentos de Enterobacterias más cercanos a la realidad y con las colonias más similares a las del medio VRBG en su versión clásica.
https://www.microkit.es/fichas/Dry-Plates-ETB-Prospecto.pdf

* 2-Ecogránulos:
Otra opción para no respirar ese horrible polvo es usar el medio deshidratado VRBG en su versión granulada que, en breve, vamos a poder ofrecer a un precio similar a su versión en polvo: https://www.microkit.es/fichas/VIOLET-RED-BILE-GLUCOSE-AGAR-VRBG-granulado.pdf

* 3-Agar MugPlus (y su versión en DryPlates®-EC):
nuestro segundo medio cromogénico, y el primero en éxito, creado desde finales del siglo pasado (1995).
Los laboratorios que lo emplean en Seilalimentos —ya sea en formato preparado, deshidratado o en DryPlates®-EC— obtienen resultados mucho más coherentes y más cercanos al valor inóculo y al valor consensuado,
en comparación con quienes utilizan VRBL para coliformes o TBX para E. coli, u otras placas deshidratadas.
https://www.microkit.es/fichas/MUGPLUS%20COLIFORM-E.COLI%20AGAR%20CCA.pdf
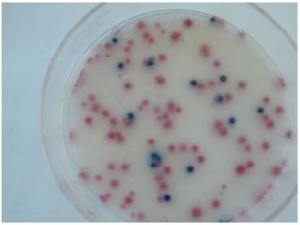

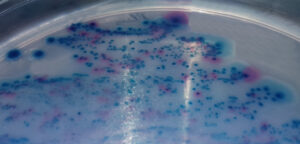
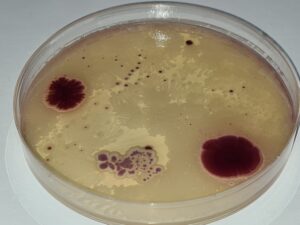
Agar MugPlus: Colonias azules: E.coli; colonias rosas: demás coliformes; resto de colores (verde, amarillo, crema…): acompañantes que no se deben incluir en el recuento de coliformes. Los coliformes son la suma de colonias azules y rosas. Ese numero a menudo es más cercano al número real de enterobacterias, que el numero de colonias obtenidas en VRBG
No es ninguna aberración:
Lo mismo que tradicionalmente el famoso MacConkey Agar se emplea para Enterobacterias cuando en realidad es un medio para coliformes (porque su fuente de carbono es la lactosa, no la glucosa)
https://www.microkit.es/fichas/Mac%20CONKEY%20AGAR.pdf
¿por qué no podemos usar un medio como el Agar MugPlus, en el que, cuando sumas las ufcs del inóculo de Enterobacterias, en servicios intercomparativos de inóculos estabilizados (como Seilalimentos),
el resultado en colonias es más cercano a esa realidad, que el resultado en colonias del VRBG?
En microbiología lo importante es la práctica, no la teoría.
Cómo abordar la incoherencia en los informes
Estas dos paradojas nos enseñan una lección clave: en nuestros PRTs de análisis y en los informes analíticos, debemos incorporar un criterio de corrección para mantener la coherencia:
* Si el número de E. coli supera al de coliformes, ajustar los coliformes al menos al mismo valor que E. coli.
* Si el número de coliformes supera al de Enterobacterias, ajustar las Enterobacterias al menos al mismo valor que los coliformes.
De no hacerlo, corremos un riesgo real: que alguien detecte la inconsistencia y se cuestione la credibilidad de nuestros resultados. No podemos aceptar sin más las limitaciones de los medios de cultivo, sino reconocerlas y corregirlas para garantizar informes coherentes.
Porque en microbiología no se trata sólo de contar colonias, sino de ofrecer certeza, fiabilidad y credibilidad. Y esa es la verdadera diferencia entre un laboratorio normal, que simplemente analiza… y uno que marca la diferencia.
Aprovechamos para indicar aquí otro tema muy importante en alimentos:
https://www.microkit.es/pdf/Listeriswabs-green-2021.pdf
Si desea conocer mejor todas estas soluciones en el recuento de Enterobacterias (DryPlates®-ETB, medio deshidratado en Ecogránulos, Agar MugPlus) solicite sus folletos técnicos y sus precios actualizados en microkit@microkit.es
¡Hasta la próxima entrega de microbiología alimentaria a finales de Junio de 2026!