Agar microbiología de aguas: medios de cultivo sólidos para elaborar placas y tubos y buscar colonias de microorganismos
Hay un avance del Siglo XX en microbiología de aguas que merece toda nuestra atención: los medios de cultivo agarizados,
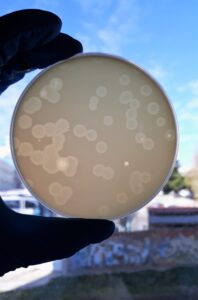
ya que gracias a este componente, extraído de ciertas algas marinas, podemos obtener colonias aisladas y éstas las podemos contar y/o identificar.
Muchos medios agarizados son simplemente su versión en caldo, a la que se añaden 10-15 g/L de agar-agar microbiológico.
Es la técnica inversa al microscopio:
en vez de introducirnos en el micromundo para ver células, hacemos que éste crezca hasta poder verlo en forma de colonias en la placa o en el tubo de medio agarizado.
Dado que la distribución de los microorganismos en cualquier muestra no es la Normal (o de Gauss) sino una «contagiosa»,
se considera que cada colonia proviene de una ufc (unidad formadora de colonia),
la cual a menudo no es una sola célula microbiana, sino varias (la madre, las hijas, las nietas… que permanecen unidas por exopolisacáridos).
A veces incluso las ufc son multiespecíficas, y eso sí que complica su identificación certera.
De modo que no es correcto hablar de colonias/g ó mL ni de ufc/placa, lo correcto es ufc/g ó mL y colonias/placa.
El agar-agar no es sólo el mejor solidificante en microbiología:
-Además tiene una elevada capacidad de tamponar
(por eso no es bueno ahorrar medio al elaborar placas y se deben añadir 18 mL/placa de 90 mm, no 15 ó 12 como hacen algunos fabricantes),
-También consigue que los medios sean menos termolábiles, como demostró MICROKIT al crear los primeros agares cromogénicos en versión deshidratada
(que ahora todo el mundo fabrica, pero antes solo había placas preparadas),
como el CCA que nosotros diseñamos y bautizamos hace ya 31 años (1995), antes de que fuera el medio oficial ISO 9308-1 para E.coli y demás coliformes, como Agar MugPlus
-Y además absorbe los metabolitos generados en el crecimiento colonial
(la curva de crecimiento de poblaciones microbianas, con fase exponencial, de meseta y degeneración, se elaboró con caldos),
lo que disminuye la fase de suicidio o alarga la fase de meseta.
Como curiosidad,
casi todo el agar microbiológico del mundo procede de la cartilaginosa alga roja Gelidium sesquipedale recolectada en Galicia, Cantabria y Asturias.

En Portugal hubo también fábricas de agar-agar antaño, pero al parecer la proporción de esta especie en sus costas no las hacía un negocio rentable.
Y en Marruecos se obtiene un agar-agar de la mezcla de algas rojas,
con lo cual su pureza es inferior y se emplea en medios de cultivo de calidad barata y sobre todo como aditivo alimentario.
Tambien en México se produce un «agar-agar microbiológico americano» desde otra alga del género Gelidium,
que resulta más blando y transparente que el agar-agar microbiológico europeo,
por lo que las fórmulas de los medios americanos suelen contener un 10% más de agar-agar/L de medio que las diseñadas con agar-agar europeo.
Muchos fabricantes europeos no lo saben y pecan de agares demasiado duros al emular las fórmulas americanas con el agar-agar de aquí,
provocando una barrera contra la oxigenación para las siembras en masa de aerobios,
(lo cual se puede aprovechar satisfactoriamente en la búsqueda de anaerobios).
Y una gran dificultad para el crecimiento colonial en la siembra por filtración de membrana:
en un agar muy duro los nutrientes no llegan bien a las ufc retenidas en la otra parte de la membrana, por lo que crean colonias diminutas que pueden pasar desapercibidas.
Y los demás agar-agar (sobre todo de Asia) se extraen de otras algas rojas (Gracilaria confervoides, incluso Chondrus crispus, que lo que contiene son carragenatos)
que no dan la talla a la hora de las siembras en masa,
ya que su punto de solidificación (54-55ºC) es muy superior al del agar-agar europeo (45-46°C),
por lo que hace inviable a buena parte de la microbiota presente (recuentos demasiado reducidos).
Además provocan heterogeneidades en la placa, montañas y valles… que dificultan una siembra eficiente de la membrana.
La lista de medios sólidos, agarizados,
es interminable, de modo que, en vez de reproducirla aqui lo mejor es ir al listado en:
https://microkit.es/fichas-tecnicas-medios-de-cultivo.htm
y buscar todos los que contienen la palabra «Agar»
o «semisólido», medios con menos proporción de agar-agar
(por ejemplo 2,7 g/L) sobre todo para permitir observar mejor la movilidad (Rappaport Semisolid Medium)
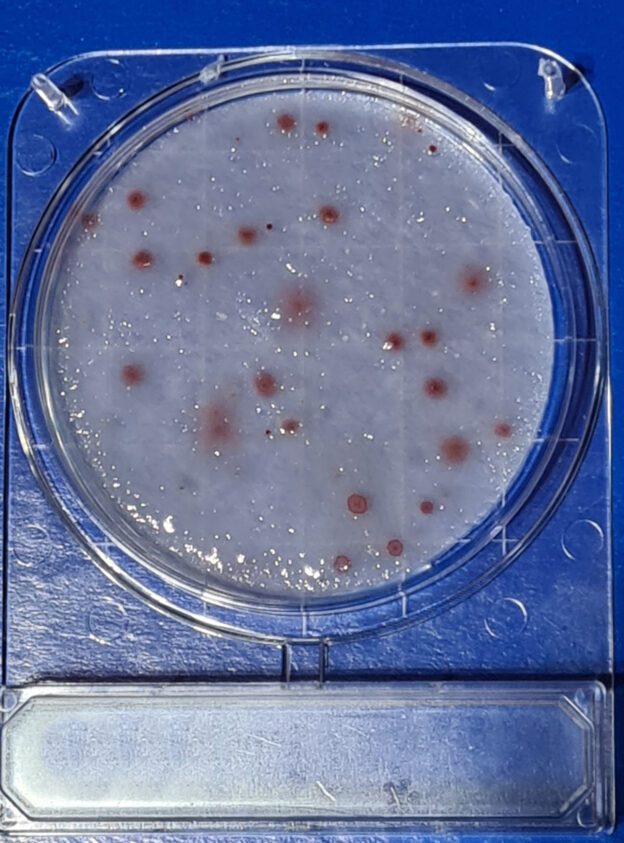
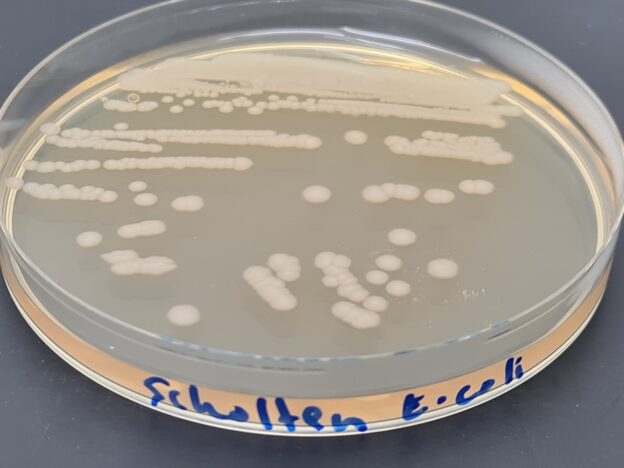
o hasta 10 g/L para una mayor opacidad del inóculo de E.coli en microbiología de aguas para detectar virus colífagos (Scholten Semisolid Medium)
Tambien los medios «Fluidos» contienen una escasa proporción de agar, para que sigan líquidos pero dificulten la oxigenación en la búsqueda de anaerobios.
No todo son ventajas
Sin embargo, el agar-agar tiene una desventaja que nos han vendido como ventaja:
no se licúa hasta alcanzar una temperatura cercana al punto de ebullición del agua
y no solidifica hasta bajar de esa temperatura a alrededor de 45ºC
Eso hace perder 1 h al dia en todos los laboratorios de microbiología del mundo que se preparan sus placas y tubos a partir de medio deshidratado
Existen otros gelificantes con ventajas e inconvenientes sobre el agar-agar;
ninguno es tan duro y transparente como el agar-agar pero
¿y si consiguiéramos uno lo suficientemente duro como para permitir convertir las ufc en colonias…
…y lo suficientemente transparente para permitir la siembra en masa sin que queden ocultas las colonias crecidas en profundidad?
Microkit lo consiguió con el HIDRAGAR. Nos costó 23 años, pero al fin lo conseguimos y de ahí surgió la posibilidad de diseñar nuestras DryPlates®,
placas preparadas que no necesitan calentar ni enfriar el medio para absorber 1 mL de muestra en masa,
pero que a la vez son las únicas placas deshidratadas del mundo que permiten realizar siembra por agotamiento en estría
¿imaginas la rapidez con que se puede hacer un análisis gracias a las DryPlates?
¡10 segundos de la muestra diluida a la estufa incubadora!
https://microkit.es/pdf/dry-plates.pdf
Tenemos en formato DryPlates® todos los medios para recuento total de aguas:
YEA (PCA water) de la ISO 6222,
R2A Farmacopea,
TSA Farmacopea,
todos ellos con un cromógeno que permite leer los resultados mucho más rápido y mejor (por contraste colonias rojas/medio crema).
Si quiere realizar un recuento en masa de aerobios de 1 mL de agua en tiempo récord,
con mucha menos manipulación (sin tener que hervir ni enfriar medios a una temperatura exacta),
con resultados sin artefactos y mucho más rápidos,
entonces aproveche la innovación y cambie a DryPlates®-TC (YEA), DryPlates®-R2 o DryPlates®-TSA Maxim.
¡tardará 10 segundos! no casi una hora como le pasa ahora con los tubos preparados que ha de fundir, atemperar, mezclar…
Solicita precios actualizados de cualquier medio agarizado o DryPlates® en microkit@microkit.es