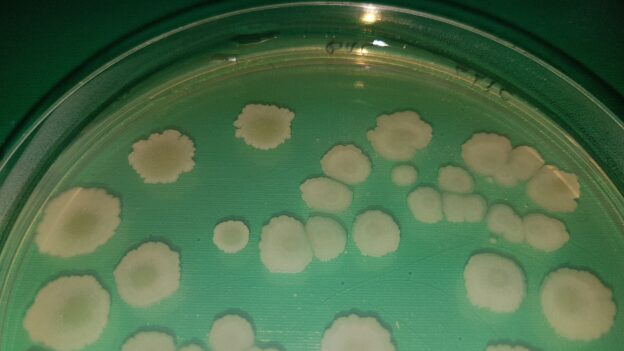
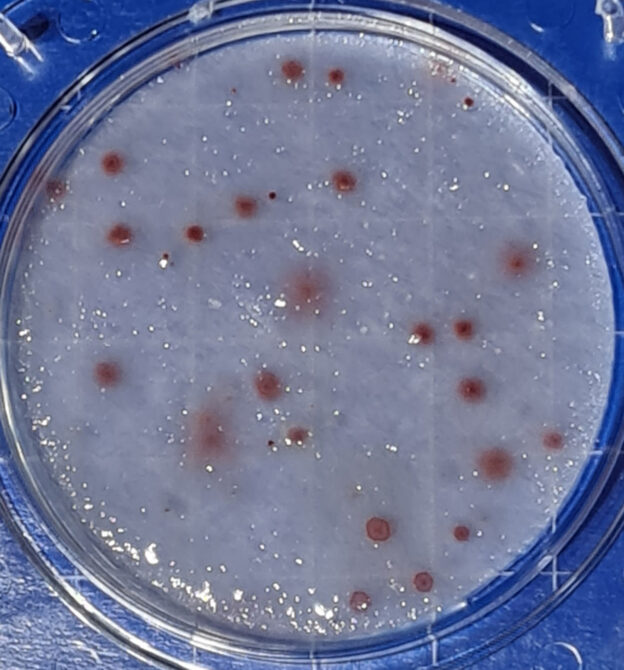
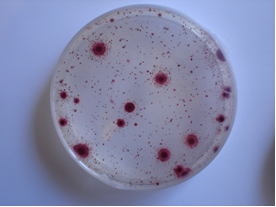
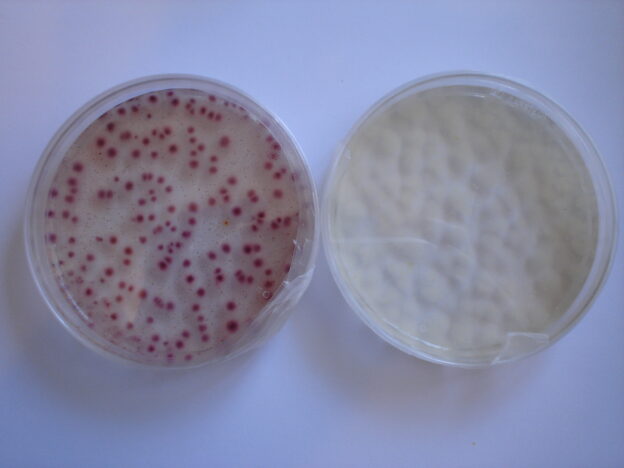
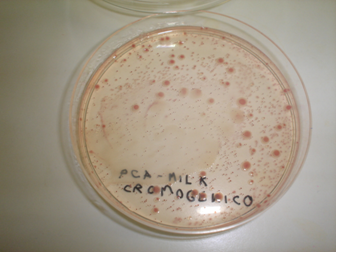
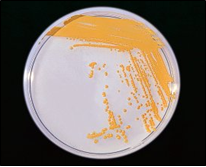
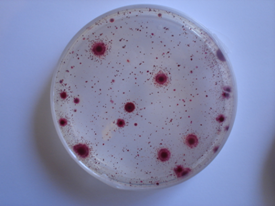
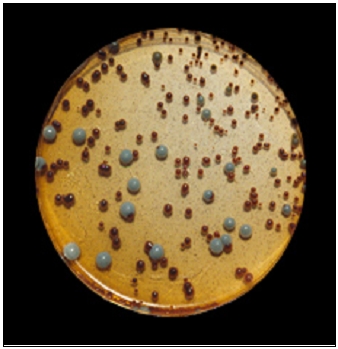
BACILLUS COAGULANS (Thermoacidurans) AGAR permite realizar el recuento de este microorganismo en alimentos y probióticos
Medio sólido diseñado para aislar y enumerar Bacillus coagulans (ahora llamado Bacillus thermoacidurans).
COMPOSICIÓN COAGULANS
- Glucosa 5 g/L
- Peptona proteosa de carne 5 g/L
- Extracto de Levadura 5 g/L
- K2HPO4 4 g/L
- Agar-agar 20 g/L
- pH final: 5 ± 0,2
Suplementos termolábiles:
- MnSO4.4H2O 0,05 mg en 10 mL de agua, esterilizar por MF y añadir al medio tras autoclavarlo
- CaCl2 0,045 mg en 10 mL de agua, esterilizar por MF y añadir al medio tras autoclavarlo
PARA USO EXCLUSIVO EN LABORATORIO. MANTENGA EL BOTE BIEN CERRADO EN LUGAR SECO, FRESCO Y OSCURO. AGITE EL BOTE ANTES DE USAR.
PREPARACIÓN
Disolver 39 g de medio en 990 ml de agua bidestilada. Calentar hasta ebullición, agitando, para su total homogeneización. Autoclavar a 121 ºC durante 15 minutos. Enfriar a 48 ºC y añadir asépticamente 10 ml del suplemento SMT041. Mezclar y repartir en placas, sin recalentar.
PRESENTACIÓN
Medio deshidratado (100 g, 500 g, 5 Kg): DMT241
Suplemento en frasco pinchable 100 mL, esterilizado por filtración, para 10 L de medio, contiene 0,05 mg MnSO4.4H2O y 0,045 mg CaCl2 cada 10 mL de agua: SMT041
NOTA
Este microorganismo es uno de los mejores probióticos que existen, porque produce ácido láctico pero, a diferencia de los lactobacilos, forma esporas resistentes. Se toma contra los trastornos intestinales (diarreas, incluyendo las diarreas de tipo infeccioso como son la diarrea por rotavirus en los niños y la diarrea del viajero; también se usa para la diarrea producida por el uso de antibióticos. El Bacillus coagulans se utiliza también para problemas digestivos en general, para el síndrome del intestino irritable (SII), para las enfermedades inflamatorias intestinales (EII, la enfermedad de Crohn y la colitis ulcerosa), para la colitis por Clostridium difficile, contra el crecimiento excesivo de bacterias «malas» en el síndrome de intestino corto y para una infección debida al Helicobacter pylori que es el que produce úlceras. Algunas personas utilizan el Bacillus coagulans para prevenir las infecciones respiratorias y para reforzar el sistema inmunológico.
Sin embargo, puede contaminar conservas alimenticias y darles un gusto ácido. Esto incluye la comida que es normalmente demasiado ácida para la mayor parte de bacterias; el B. coagulans (thermoacidurans) puede crecer en un pH tan bajo como 4,2. Este medio también sirve para detectar Clostridios acidófilos que estropean ciertos alimentos envasados.
CONTROL DE CALIDAD DEL AGAR BACILLUS COAGULANS
Es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio, tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…)
DESHIDRATADO: Polvo grueso, Color crema. PREPARADO: Estéril, Color paja.
EVALUACIÓN DEL RENDIMIENTO ISO/TS 11133-2: 24-48 h a 30-37 ºC, aplicando el método ISO 7932, o el indicado en el Manual MICROKIT actualizado:
- Bacillus coagulans (thermoacidurans) WDCM 00002, Excelente, PR > 90% de colonias respecto al número de ufc certificadas e inoculadas en TSA
- Bacillus subtillis MKTA 6633, crecimiento excelente.
SIEMBRA
Sembrar 0,1 ml de la muestra y su serie de diluciones decimales, en superficie, repartiendo con el asa de Digralsky (VRR154, desechables VCL155). Incubar a 37 ºC aproximadamente, durante 24-72 horas. Al no ser un medio selectivo, deben identificarse las colonias que, si proceden de conservas ácidas, es muy probable que se trate de esta especie y si proceden de inóculos puros, el medio sirve para enumerar y conocer la concentración del preparado probiótico.
El usuario es el único responsable de la eliminación de los microorganismos según la legislación medioambiental vigente. Autoclavar antes de desechar a la basura.
https://www.microkit.es/fichas/BACILLUS-COAGULANS-THERMOACIDURANS-AGAR.pdf
Si desea más información sobre nuestros BACILLUS COAGULANS (Thermoacidurans) AGAR rellene nuestro formulario de contacto http://www.medioscultivo.com/contacto . O si lo prefiere póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16
https://www.microkit.es/monograficos/10-Bacillus-monograf–a.pdf