SPS AGAR (Sulfite Polimixin Sulfadiacin Agar)
Medio selectivo para la detección y recuento de Clostridium sulfito-reductores en alimentos y aguas
Métodos AOAC – ICMSF – UNE 13401 – UNE-EN 26461
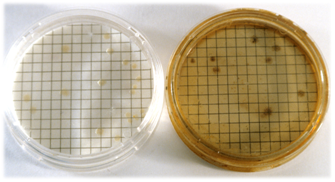
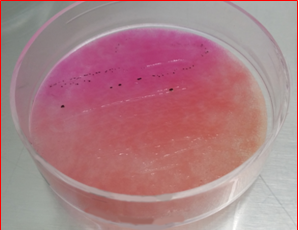
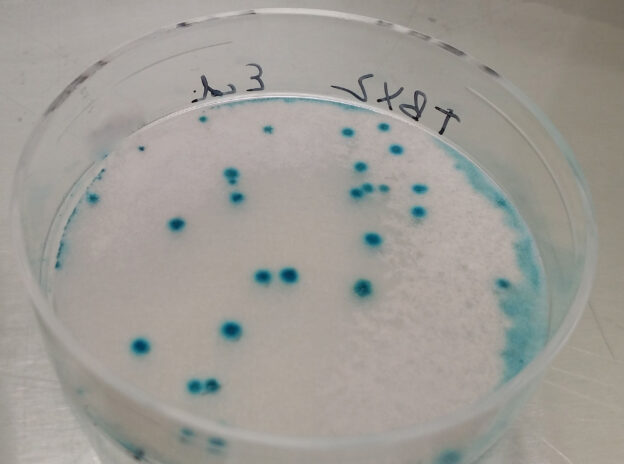
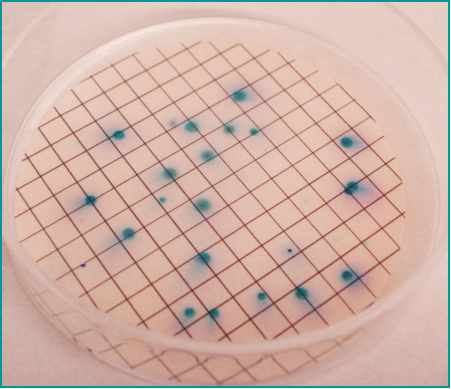
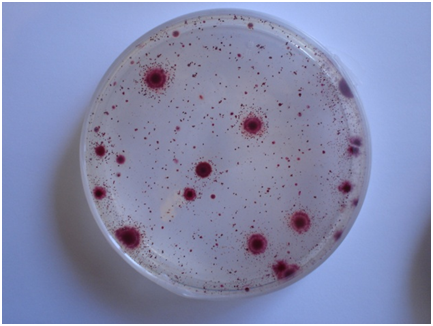
Clostridios sulfito-reductores en SPS Agar
DESCRIPCIÓN GENERAL
El SPS Agar (Sulfite Polimixin Sulfadiacin Agar) es un medio selectivo diferencial utilizado para la detección, aislamiento y recuento de Clostridium sulfito-reductores, incluyendo Clostridium perfringens y Clostridium sporogenes, en alimentos, aguas y muestras ambientales.
Basado en las recomendaciones de la AOAC y del ICMSF, este medio permite la identificación visual de los clostridios por la reducción de sulfito a sulfuro, que reacciona con el citrato férrico produciendo colonias gris-negras características.
Es un medio de alta selectividad y sensibilidad, gracias a la acción combinada de Polimixina B y Sulfadiacina, que inhiben flora acompañante no clostridial.
COMPOSICIÓN (por litro)
| Componente | Cantidad |
|---|---|
| Peptona de caseína | 15,00 g |
| Extracto de levadura | 10,00 g |
| Citrato de hierro | 0,80 g |
| Sulfito sódico | 0,50 g |
| Polimixina B (sulfato) | 0,01 g |
| Sulfadiacina sódica | 0,12 g |
| Agar-agar | 13,90 g |
pH final: 7,0 ± 0,1
PREPARACIÓN DEL MEDIO
-
Disolver 40 g de medio en 1 litro de agua destilada.
-
Calentar agitando hasta ebullición para su completa disolución.
-
Repartir en tubos o frascos.
-
Autoclavar a 121 ºC durante 15 minutos, o preferiblemente a 116 ºC durante 15–30 minutos.
-
Enfriar rápidamente en baño de agua fría.
Recomendación: El autoclavado a 116 ºC es preferible, ya que preserva la sensibilidad del medio.
Utilizar inmediatamente tras la preparación para evitar su oxigenación, que resulta letal para los clostridios.
Suplemento opcional: Para potenciar la formación de colonias negras, añadir 1 vial del suplemento estéril VMT136 por cada 100–1000 ml de medio estéril, hervido y enfriado a 45–50 ºC.
Nota: Las partículas negras que pueden aparecer al enfriar son normales y aumentan la sensibilidad del medio, conforme a las normas UNE 13401 y UNE-EN 26461.
CONDICIONES DE ALMACENAMIENTO
-
Uso exclusivo en laboratorio.
-
Mantener el bote bien cerrado, en lugar seco, fresco y oscuro.
Código: BCD901
Aspecto del producto:
-
Deshidratado: Polvo beige.
-
Preparado: Medio estéril, color crema-blanquecino.
CONTROL DE CALIDAD DEL MEDIO
El control de calidad se realiza en nuestro laboratorio. Se recomienda repetirlo en el suyo si han cambiado las condiciones ambientales (tiempo prolongado sin uso, altas temperaturas, desinfección reciente, etc.).
Ensayo de rendimiento (24 h a 37 ºC en anaerobiosis)
| Microorganismo | Resultado esperado | Recuento relativo (PCA estándar*) | Observaciones |
|---|---|---|---|
| Clostridium sporogenes MKTA 11437 | Colonias gris-negras | 240–347 % | Selectivo y diferencial. |
| Clostridium perfringens MKTA 13124 | Colonias gris-negras | 110–420 % | Selectivo y diferencial. |
| Staphylococcus aureus MKTA 6538P | Inhibido | — | Sin crecimiento. |
| Escherichia coli MKTA 25922 | Inhibido | — | Sin crecimiento. |
* PCA estandarizado con recuperación ≥92–125 % respecto a cepas trazables a la colección tipo.
Las variaciones detectadas entre lotes se deben principalmente a las cepas inoculadas, no al medio.
PRESENTACIÓN DISPONIBLE
-
Tubos preparados (parafinados de 9 ml o sin parafina de 18 ml)
-
Frascos parafinados de 50 ml (doble concentración)
-
Frascos de 100 ml y 250 ml
-
Medio deshidratado
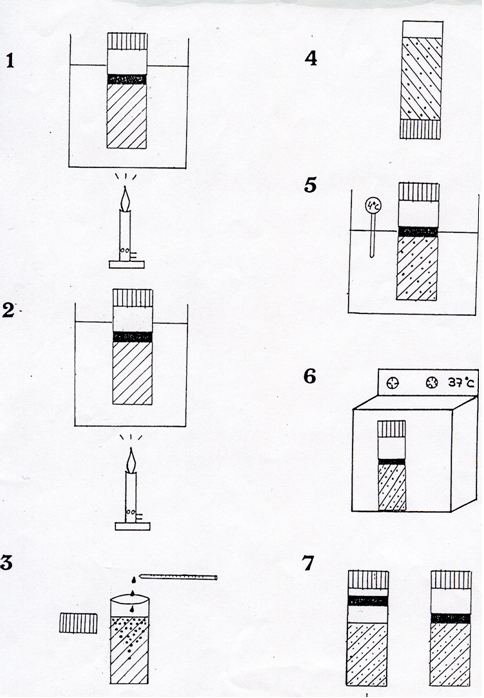
- Tubo y frasco de SPS Agar parafinado

SIEMBRA Y CONDICIONES DE INCUBACIÓN
Método recomendado: Siembra en profundidad (placas, tubos o frascos).
-
Para detectar esporas, calentar la muestra a 98 ºC, enfriar a 75 ºC y añadir 1 ml al tubo o frasco con el medio fundido.
-
Mezclar suavemente (sin agitar) para evitar oxigenación.
-
Enfriar en posición vertical (en tubos parafinados, la parafina solidifica en la superficie, creando anaerobiosis).
-
Para detección en aguas, usar frascos parafinados a doble concentración e inocular 20–50 ml de muestra.
-
Incubar a 35–37 ºC durante 24 horas en anaerobiosis.
Alternativa práctica: Inocular 1 ml sobre un tubo hervido y enfriado a:
-
75 ºC → detección de esporas
-
45 ºC → detección de formas vegetativas
Cerrar, voltear sin agitar, incubar en vertical y contar directamente las colonias negras que crecen en anaerobiosis (excepto los 3–5 mm superiores, oxigenados).
INTERPRETACIÓN DE RESULTADOS
-
Colonias negras: Clostridium sulfito-reductores confirmados.
-
Colonias blancas: Presuntivas (anaerobiosis insuficiente).
El ennegrecimiento del medio se debe a la reducción del sulfito sódico a sulfuro, que precipita con el citrato férrico, generando un color gris o negro característico.
GESTIÓN DE RESIDUOS
El usuario final es responsable de eliminar los microorganismos conforme a la legislación medioambiental vigente.
Autoclavar los materiales antes de su eliminación.
INFORMACIÓN ADICIONAL
Monográfico sobre Clostridium perfringens y clostridios sulfito-reductores (PDF)
Correo: microkit@microkit.es
Teléfono: 91 897 46 16
Esquema sobre el uso de los tubos de SPS Agar parafinados, realizado en 1989