BACILLUS SPOROTHERMODURANS AGAR HRS PERMITE LA DETECCIÓN Y RECUENTO DE ESPORAS RESISTENTES A ALTAS TEMPERATURAS HRS (EJ:TETRABRICKS)
HRS BACILLUS SPOROTHERMODURANS AGAR
INTRODUCCIÓN
La presencia de esporas altamente resistentes al calor de Bacillus sporothermodurans en leche pasterizada por el método Ultra Hight Temperature (UHT) se ha convertido en un problema importante en la industria láctea.
Su presencia se considera indeseable, ya que obstaculizan los requisitos de esterilidad comercial.
En un estudio (APPLIED AND ENVIRONMENTAL MICROBIOLOGY, Mar. 2005, p. 1480–1494), se han evaluado, mediante el uso de un selectivo tratamiento térmico de 30 minutos a 100°C, la presencia, fuentes, y naturaleza de las esporas potencialmente muy resistentes al calor en la leche cruda.
Se detectaron altos números de estas esporas en la tela del filtro del equipo de ordeño y en muestras de cultivos y forrajes verdes.
Se aislaron aproximadamente 700 cepas después del calentamiento selectivo. La colección de cepas mostró una notable diversidad, con representantes de siete géneros que forman esporas aerobias.
Las más frecuentes esporas aisladas de leche UHT han sido Bacillus sporothermodurans (aerobio facultativamente anaerobio), Brevibacillus borstelensis, Paenibacillus lactis, Bacillus sphaericus, Bacillus licheniformis, y Brevibacillus brevis.
El 23% de las 603 cepas formadoras de esporas pertenecen a 18 nuevas especies.
REDUCCIÓN DE CARGA
La reducción de esta carga de esporas por buenas medidas higiénicas durante el ordeño probablemente podría reducir aún más el nivel de contaminación de la leche cruda…
…y de esta manera reducir al mínimo el recuento aeróbico de formadores de esporas de bacterias que podrían conducir al deterioro de la leche y los productos lácteos.
Las HRS (Heat Resistant Spores) o más coloquialmente “termorresistentes”, aparecen en muestras de leche UHT, sobre todo si el método de tratamiento térmico es “indirecto” (intercambiador de calor).
Los métodos “directos” con inyección de vapor sobrecalentado son más eficaces, pero estas esporas también aparecen de vez en cuando.
No son un problema para la salud (son microorganismos de riesgo biológico 1: sin riesgo para la salud) y aparentemente no alteran la leche, de modo que nos hemos acostumbrado a beber leche contaminada por estos microorganismos.
El problema no es para el consumidor sino para la imagen de la industria.
SOLUCIONES
MICROKIT ha desarrollado un medio de cultivo cromogénico, derivado del Plate Count Agar ISO 4833, con factores “doping” que permiten la visión de estas esporas germinadas en forma de colonias, que suelen ser diminutas y rojas, gracias a un cromógeno termoestable.
El medio no es selectivo para B. sporothermodurans, de modo que también crecen en el mismo Bacillus licheniformis, Bacillus sphaericus y los demás esporulados alterativos de la leche UHT:
Las esporas termorresistentes (HRS).
Pero se denomina así por el mayor conocimiento que tiene la industria láctea de la denominación “B. sporothermodurans” que de las siglas HRS.
COMPOSICIÓN
- Triptona 5,0 g
- Extracto de Levadura 2,5 g
- Glucosa 1,0 g
- Factores doping MICROKIT 8,0 g
- Agar‑agar 10,5 g
- Cromógeno termoestable c.s.
- (Fórmula por litro)
- pH final: 6,8 ± 0,2
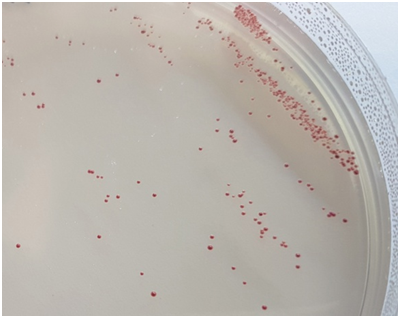
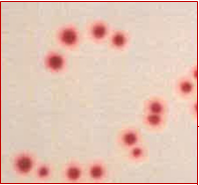
Obsérvese la forma de volcán de las colonias, rojas, de Bacillus sporother-modurans
PREPARACIÓN
Disolver 27 g de medio en 1 litro de agua destilada.
Calentar hasta ebullición, agitando para su completa disolución.
Repartir en tubos o frascos. Autoclavar a 121 ºC durante 15 min o preferiblemente a 116°C durante 15 minutos. No sobrecalentar ni mantener fundido mucho tiempo. Refundir sólo una vez. El color final del medio es blanco-crema.
A veces, por sobrecalentamiento, adquiere un tono rosado que retorna al crema cuando se vuelve a enfriar el medio, lo cual no afecta los resultados.
Si lo desea, puede añadir trazas de vitamina B12 cuando el medio se está enfriando a 47-50ºC, aunque ya están incorporadas en el medio deshidratado.
Si prefiere obtener colonias grandes, añada 37 g/L de BHI Broth (MICROKIT DMT022). Si desea una cierta selectividad en leche cruda, añada a 1 L de medio, cuando se está enfriando a 47-50ºC, 10 ml de un frasco pinchable de polimixina B (MICROKIT SMS009).
O mejor aún: someta a la leche cruda a un calentamiento UHT para eliminar toda la flora acompañante.
PARA USO EXCLUSIVO EN LABORATORIO. MANTENGA EL BOTE BIEN CERRADO EN LUGAR SECO, FRESCO Y OSCURO. AGITE EL BOTE ANTES DE USAR.
DESHIDRATADO CODIGO: DMT532
CONTROL DE CALIDAD DEL MEDIO
Realizado en nuestro laboratorio; es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio, tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…). DESHIDRATADO: Polvo grueso, Crema PREPARADO: Estéril, Crema
EVALUACIÓN DEL RENDIMIENTO ISO/TS 11133-2 24-72 h a 37-55 ºC o bien 3-5 días a 30 ºC, aplicando el método ISO 4833, ISO 2293, o el indicado en el Manual MICROKIT:
- Bacillus sporothermodurans MKTD 10599, Excelente, pequeñas colonias rojas o fucsia, redondas, con forma de volcán (boina), PR >90% de colonias respecto al TSA.
- Bacillus subtilis WDCM 00003, Excelente, colonias grandes, rojo burdeos, lobuladas, PR >90% de colonias respecto al número de ufc certificadas e inoculadas en TSA.
- Bacillus cereus WDCM 00001, Excelente, colonias céreas, fucsia, enormes, lobuladas, PR >90% de colonias respecto al número de ufc certificadas e inoculadas en TSA.
- Enterococcus faecalis WDCM 00009, Excelente, colonias pequeñas, rojas, redondas, con márgenes incoloros, PR >90% de colonias respecto al TSA.
- Staphylococcus aureus WDCM 00032, Excelente, colonias rojo burdeos, grandes, redondas, mucosas, PR >90% de colonias respecto al TSA.
Las colecciones TIPO prohíben el uso de su referencia, por lo que indicamos la Universal WDCM según ISO 11133-2:2014 y la Colección de Cepas Nativas Tropicales.
PRESENTACIÓN:
MEDIO DESHIDRATADO (100 g, 500 g, 5 Kg).
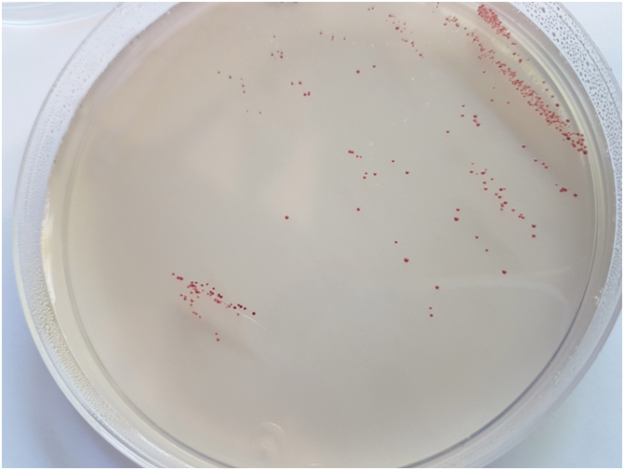
Recuento total de bacterias esporuladas en leche UHT y otros alimentos UHT (lácteos, gelatina, forraje…).
Las colonias crecen en distintos tonos del rojo: rosa, naranja, púrpura…. sobre el tono crema del medio (excepto ciertos acidolácticos y ciertas levaduras, que crecen con colonias blancas, sin viraje, por lo que este medio los distingue de los aerobios).
El color de las colonias no afecta a las pruebas de identificación posteriores que quisiera realizar.
MODO DE EMPLEO
Inocular 1 ml de muestra de leche y su serie de diluciones decimales, en masa, para detectar precozmente la posible contaminación del lote, con esporas de este microorganismo (o bien estriar en superficie muestras ya alteradas).
Si se desea analizar la leche antes de la UHT, añada a cada L de medio 10 ml de Polimixina B (frascos pinchables MICROKIT SMS009), cuando está enfriándose a 47-50ºC, para eliminar buena parte de la flora acompañante.
La polimixina es un antibiótico polipeptídico producido por una cepa de Bacillus polymyxa, activo frente a Gram negativos, ya que rompe violentamente su membrana plasmática. Atención: los iones Ca++ inhiben su acción.
Aunque el mejor agente selectivo es el calor UHT, para buscar sólo sus supervivientes, con este medio (sin suplementos de antibióticos).
De modo que para analizar leche cruda, es mejor someterla a un calentamiento similar a UHT antes de sembrarla en el medio de cultivo, a fin de eliminar la flora acompañante.
Incubar una placa a 30 ºC aproximadamente durante 3-5 días, e incubar otra placa a 37 y/o 55 ºC aproximadamente, durante 48-72 horas.
INTERPRETACIÓN DE RESULTADOS
Buscar las colonias rojas y pequeñas típicas de B.sporothermodurans, aunque cualquier otro tipo de colonia que aparezca, también demuestra una UHT deficiente.
La recuperación supera el 20% por encima de la obtenida en PCA y el 16% por encima de la obtenida en TSA, gracias a ciertos factores doping descubiertos y agregados por MICROKIT.
Esta fórmula, con menos agar, aumenta la sensibilidad del medio frente a los aerobios más lábiles, al permitir una mejor oxigenación del fondo de la placa.
Este medio está diseñado para siembra en masa de productos que han sufrido esterilización UHT, de modo que los resultados no son concluyentes en productos no-UHT, con numerosos falsos positivos (sobre todo si no se añade polimixina B).
Si desea sembrar en superficie, utilice 32 g/l de este mismo medio, en lugar de 27 g/l.
Para minimizar la desecación en muestreos de aire y superficies, o para siembra en Spiral, añadir 2 gotas de antiburbujas (MICROKIT SBL001) por cada litro de agua, antes de añadir el medio y antes de autoclavar.
https://www.microkit.es/fichas/HRS-RAPID-Cromogenic-sporothermodurans-Agar.pdf
https://www.microkit.es/monograficos/10-Bacillus-monograf–a.pdf
ANEXO FOTOGRÁFICO

B.sporothermodurans en Maxim Agar Cromogénico (MICROKIT BCD515) en 3 días a 35ºC

B.sporothermodurans en HRS cromogénico (MICROKIT DMT532). Obsérvese el mayor tamaño de las colonias en 3 días a 35ºC, que con lupa ya muestran su forma de volcán

B.sporothermodurans en HRS cromogénico (MICROKIT DMT532) al que hemos añadido 37 g/L de BHI Broth (MICROKIT DMT022). Obsérvese el espectacular tamaño de las colonias en 3 días a 35ºC, que muestran a simple vista su forma de volcán

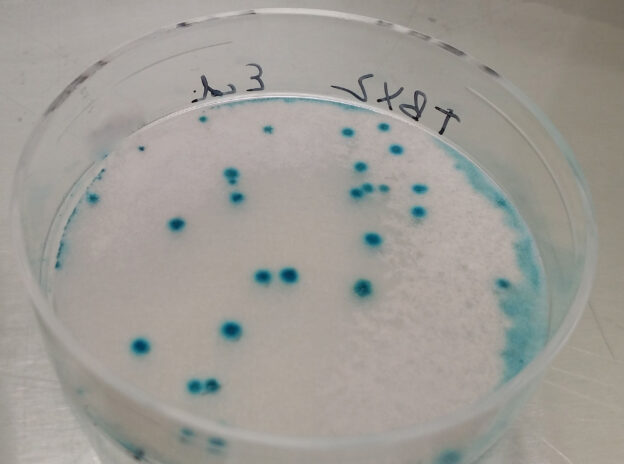
Mix de Acidolácticas en HRS cromogénico con polimixina (MICROKIT DMT532+SMS009): Colonias blancas o muy ligeramente rosadas
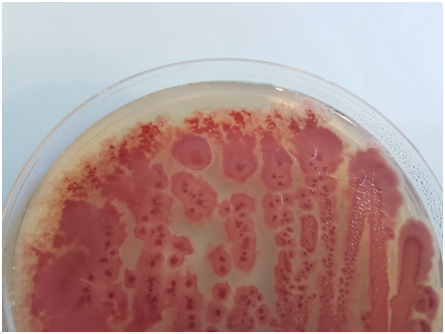
Bacillus cereus en HRS cromogénico con polimixina (MICROKIT DMT532+SMS009): Colonias céreas, enormes, fucsia, lobuladas

Bacillus subtilis en HRS cromogénico con polimixina (MICROKIT DMT532+SMS009): Colonias grandes, rojo burdeos, lobuladas
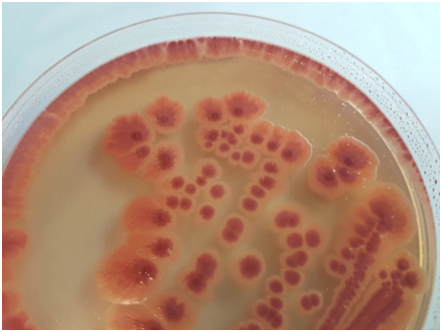
Bacillus subtilis en HRS cromogénico con polimixina (MICROKIT DMT532+SMS009) al que hemos añadido 37 g/L de BHI Broth (MICROKIT DMT022): Colonias enormes, fucsia, lobuladas

Enterococcus faecalis en HRS cromogénico con polimixina (MICROKIT DMT532+SMS009): Colonias pequeñas, redondas, con centro rojo y borde incoloro, aspecto similar a Listeria monocytogenes

Listeria monocytogenes en HRS cromogénico con polimixina (MICROKIT DMT532+SMS009): Colonias pequeñas, redondas, con centro rojo y borde incoloro, aspecto similar a Enterococcus faecalis

Staphylococcus aureus en HRS cromogénico con polimixina (MICROKIT DMT532+SMS009): Colonias grandes, rojo burdeos, mucosas, redondas

Shigella flexneri en HRS cromogénico con polimixina (MICROKIT DMT532+SMS009): único Gram negativo testado que crece, con colonias enormes, fucsia, lobuladas
CONCLUSIÓN
BACILLUS SPOROTHERMODURANS AGAR HRS PERMITE LA DETECCIÓN Y RECUENTO DE ESPORAS RESISTENTES A ALTAS TEMPERATURAS HRS (EJ:TETRABRICKS)
https://www.microkit.es/fichas/HRS-RAPID-Cromogenic-sporothermodurans-Agar.pdf
El usuario es el único responsable de la eliminación de los microorganismos según la legislación medioambiental vigente. Autoclavar antes de desechar a la basura.
Si desea más información sobre nuestro BACILLUS SPOROTHERMODURANS CROMOKIT AGAR (HRS CROMOGENIC AGAR) póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es
Prepárese para más de una sorpresa informativa cuando vea nuestro video sobre los medios Cromogénicos: https://www.youtube.com/watch?v=-JVPVWxY8ZE&t=271s