DESINFECTEST – LAMINOCULTIVOS “dipslides” para control microbiológico industrial y ambiental de superficies y de líquidos con alta carga microbiana potencial https://www.microkit.es/pdf/desinfectest.pdf

INTRODUCCIÓN
DESINFECTEST® es la más moderna gama de laminocultivos de MICROKIT.
Se trata de kits listos para su uso que permiten el análisis microbiológico de líquidos crudos, de superficies y de colonias obtenidas en medios de cultivo generales.
Han sido especialmente diseñados para industria.
Están formados por una lámina que se inserta en el tapón de un tubo hermético y transparente.
La lámina está rellena, por cada cara, de un medio de cultivo convexo, de ahí el nombre que le aplicamos de laminocultivo (en inglés, «dipslide»). La palabra laminocultivo la inventamos en 1998 y desde entonces se ha extendido hasta ser la forma oficial de denominarlos (lo mismo que dipslide lo es en inglés)
Cada tipo de DESINFECTEST® tiene dos medios de cultivo diferentes, uno en cada cara, específicos cada uno para un tipo de análisis, general o selectivo (ver la gama mas adelante).
Por su sencillez, DESINFECTEST® pueden ser utilizado por personal no especializado, tanto en trabajo de campo como de laboratorio.
Los resultados obtenidos son perfectamente comparables a los de los métodos convencionales siempre que se sigan las instrucciones al pie de la letra.
DESINFECTEST® se basa en el principio de que todo microorganismo, alimentado por el medio agarizado adecuado a una temperatura y en un tiempo concretos, da lugar a una colonia característica que es observable a simple vista.
Para el análisis de líquidos crudos la ventaja es la comodidad y el ahorro de diluciones siempre que la contaminación esté entre 1.000 y 10.000.000 de microorganismos por mililitro.
El apéndice final de la lamina permite que el líquido sobrante tras la inmersión resbale y no se acumule al final del medio de cultivo,
lo que impide que se obtengan recuentos falseados y heterogéneamente distribuidos en el medio de cultivo, como sucede en otros laminocultivos peor diseñados.
Para el análisis de superficies, la ventaja frente a las Placas de Contacto o Rodac (ENVIROCOUNT®) es que el sistema hermético permite transportar el kit sin necesidad de un especial cuidado, incluso para análisis de campo.
Y que al tener el medio 2 x 10 cm en vez de 50 x 50 cm, permite muestrear superficies cóncavas, como el interior de reactores y tubos.
Para el análisis de colonias obtenidas en medios de cultivo generales, DESINFECTEST® es una forma económica, y con larga caducidad, de tener un pequeño stock de medios de cultivo selectivos que nos orientarán sobre el tipo de microorganismo que hemos encontrado:
Aerobio,
Enterobacteria,
Coliforme,
Salmonella,
E. coli,
Levadura,
Moho
u otro.
El conjunto de los diversos tipos de DESINFECTEST® se convierte así en una batería de preidentificación de microorganismos.
LA SENSIBILIDAD DE LOS DIPSLIDES ES DE HASTA 1 ufc/mm2 EN SUPERFICIES
Y DESDE 1.000 ufc/ml EN MUESTRAS LIQUIDAS.
Todo usuario de DESINFECTEST®, conoce las ventajas de este producto, que lleva más de tres décadas resolviendo los problemas de control microbiológico de superficies y de líquidos crudos, en cientos de usuarios de España, resto de Europa y otros países.
Los DESINFECTEST® tienen la lámina flexible para poder analizar superficies más cómodamente.
Y su producción a nivel industrial limita las contaminaciones y deslaminaciones a niveles prácticamente nulos.
GAMA
DESINFECTEST® Referencia Medios-Utilidad Color Medio
AEM/AET MBN101 TSA Neutralizing Agar TTC (AET) Incoloro
PCA + TTC-Recuento total (AEM) Incoloro
EC MBN103 Salmonella Cromogenic Agar Crema
Coliformes + E. coli Cromogenic Agar Crema
ARICPC MBN200 Neutralizing Agar incoloro +TTC (AET) Incoloro
VRBG Agar + Inactivadores (E) Púrpura
MIX MBN407 Neutralizing Agar incoloro +TTC (AET) Incoloro
Rosa Bengala Caf.-Hongos ambientales (LM) Rosa
MODO DE EMPLEO
Leer además las instrucciones del tipo concreto de DESINFECTEST® con el que se va a trabajar, especificadas más adelante.
1.‑ Para líquidos:
Desenroscar el tapón e introducir la lámina en la muestra durante un instante (máximo 5 segundos).
La calidad de la muestra no se ve afectada por la inmersión del laminocultivo, que es estéril y no contiene productos tóxicos.
 Si se dispone de poco volumen de muestra, dejarla gotear sobre cada medio de cultivo con la ayuda de una pipeta Pasteur (MICROKIT VFR273)
Si se dispone de poco volumen de muestra, dejarla gotear sobre cada medio de cultivo con la ayuda de una pipeta Pasteur (MICROKIT VFR273)
El mismo tubo del laminocultivo puede servir de recipiente para ser llenado con el líquido de muestra y sumergir allí la lámina agarizada.
En tal caso no debe olvidarse vaciarlo tras la inmersión.

Si el líquido es muy espeso, o incluso si se trata de un sólido previamente desmenuzado, debe diluirse a razón de 10 ml o 10 g) en un frasco de 100 ml de Agua Peptonada Tamponada (MICROKIT RPL007)
y luego multiplicarse por 10 los resultados obtenidos.
Si la muestra se prevé muy contaminada (con más de 1.000.000 microorganismos por mililitro) debe diluirse 1 ml en un frasco de 100 ml de Agua Peptonada Tamponada estéril (MICROKIT RPL007)
y luego multiplicarse por 100 los resultados obtenidos.
Si la muestra se prevé poco contaminada (con menos de 1.000 microorganismos por ml) se recomiendan otros métodos:
DryPlates® de MICROKIT,
aunque si sólo se precisa ver presencia/ausencia de algún microorganismo, puede enriquecerse en un caldo selectivo antes de usar el DESINFECTEST®.
En cualquier caso, dejar escurrir el líquido sobrante, depositando el apéndice del final de la lámina sobre un papel secante.
No agitar nunca.
Volver a enroscar el laminocultivo en su tubo sin apretar al máximo.
Incubar en posición vertical, preferiblemente con el tapón arriba, el tiempo y a la temperatura indicados mas adelante para cada tipo de DESINFECTEST®.
2.‑ Para control de superficies:
Desenroscar el tapón con cuidado de no tocar los medios de cultivo con los dedos.

Tocar con un medio de cultivo la superficie de análisis, ejerciendo una ligera presión y sin desplazarlo, durante unos instantes (mejor unos 10 segundos).
Puede apoyarse un dedo de la otra mano en la lengüeta final.
Repetir la operación con el otro medio en una superficie muy cercana a la primera, pero nunca exactamente en la misma.
La flexibilidad de la lámina permite acceder a superficies difíciles sin necesidad de desmontarla del tapón.
Si la superficie de análisis es rugosa, curva muy pronunciada o de difícil acceso, rascarla con una torunda estéril previamente humedecida en Ringer
y, después, hacerla girar sobre la superficie de un medio extendiendo el inóculo por toda la superficie del agar.
Repetir la operación con otro escobillón para el otro medio de cultivo.
Volver a enroscar el laminocultivo en su tubo sin apretar al máximo para que haya intercambio con el aire.
Incubar en posición vertical, preferiblemente con el tapón arriba, el tiempo y a la temperatura indicados más adelante para cada tipo de DESINFECTEST®.
3.‑ Para identificación de colonias:
Las colonias obtenidas en medios de cultivo generales pueden identificarse mediante dos pasos sucesivos:
1 Uso de medios de cultivo selectivos orientativos del tipo de microorganismo.
2 Identificación de las colonias aparecidas en éstos con kits bioquímicos e inmunológicos específicos (ver para cada tipo de DESINFECTEST® explicado más adelante) y consultar al servicio técnico de MICROKIT, folleto Pre-Ident: https://www.microkit.es/pdf/pre-identificacion.pdf
Los medios de cultivo selectivos más rentables desde el punto de vista economía/caducidad son los laminocultivos. Por ello, tener un stock de una caja de cada tipo de DESINFECTEST® cada semestre, puede sacar de apuros a muchos laboratorios que habitualmente centran sus análisis en el recuento total.
La colonia obtenida en el medio de cultivo general (TSA, Maxim Agar, PCA, PCA-Cromogénico, LPT100 Agar, Letheen, Eugon, Nutrient Agar, PCA‑Carbón, D/E Neutralizing Agar …) se toma con la ayuda de un asa de siembra estéril y se introduce en un tubo de 9 ml de Buffered Peptone Water (MICROKIT TPL007).
Se agita bien y se deja reposar unos minutos.
Se introduce un asa calibrada hasta la mitad del tubo, se saca y se deja gotear, sin agitar.
La película que queda en el círculo del asa se extiende en zig zag sobre una cara del laminocultivo, recorriendo la mayor extensión posible, sin pasar dos veces por el mismo punto, a fin de obtener colonias aisladas que luego puedan utilizarse en la identificación bioquímica o inmunológica.
Se repite la operación con la misma asa calibrada estéril en la otra cara del laminocultivo, y así sucesivamente en los demás medios del resto de DESINFECTEST®.
O mejor coin PLAQUIS® herméticas, cuya gama es completísima y tienen 6 meses de caducidad: https://www.microkit.es/pdf/plaquis.pdf
Se cierra y se incuba cada laminocultivo en posición vertical, preferiblemente con el tapón arriba, el tiempo y a la temperatura indicados más adelante para cada tipo de DESINFECTEST®
LECTURA DE RESULTADOS
(Leer además las instrucciones del tipo concreto de DESINFECTEST® con el que se va a trabajar, especificadas más adelante).
Tras la incubación recomendada en cada tipo de DESINFECTEST®, se compara visualmente la concentración de colonias de cada medio con las tablas de resultados incluidas en cada caja de DESINFECTEST®.
1.‑ Para líquidos:
Los resultados obtenidos aquí serán semicuantitativos.
Existe una clara correlación entre la densidad de colonias desarrolladas en un laminocultivo y el número de microorganismos por mililitro que hay en la muestra (Mossel, Genner, etc).
Comparar la densidad de colonias de cada medio con las tablas de resultados incluidas en cada caja de DESINFECTEST®.


Así obtendremos el orden de magnitud de contaminación en valores exponenciales de 10 (1.000, 10.000, 100.000, 1.000.000…) cfu/ml.
Si es superior a los valores permitidos por la legislación o por las normas internas del laboratorio para el producto concreto, el lote no es válido.
En caso contrario, tampoco debe olvidarse que es necesario continuar con los controles de forma rutinaria, al menos uno por cada lote.
Si el valor obtenido es superior a 100.000 cfu /ml en bacterias o levaduras, o a 30 colonias/cara en mohos, conviene repetir el test a partir de una dilución de la muestra en Agua Peptonada Tamponada estéril (MICROKIT RPL007),
y luego multiplicar el resultado obtenido por el factor de dilución
Para los medios selectivos, no se suele buscar recuento, sino presencia o ausencia de alguna colonia a partir de caldos de enriquecimiento.
2.‑ Para control de superficies:
Los resultados obtenidos aquí serán cuantitativos.
Cada colonia ha crecido a partir de un microorganismo inicial (o de una ufc).
Por tanto, el número de colonias de cada cara indica el número de microorganismos que había en los 10 cm2 de superficie analizados con cada medio.
Con las tablas de resultados se facilita el recuento para los valores altos:
Comparar la densidad de colonias de cada cara con las tablas de resultados incluidas en cada caja de DESINFECTEST®

BACTERIAS Y LEVADURAS
Arriba, ufc/ml de muestra líquida.
Abajo, ufc/cm2 de muestra de superficies.
≤1×103 5×103 1×104 1×105 1×106 ≥1×107

MOHOS FILAMENTOSOS
Arriba, ufc/ml de muestra líquida.
Abajo, ufc/cm2 de muestra de superficies.
ligera moderada importante
Deben servir de alerta resultados superiores a 40 microorganismos por cara en superficies de trabajo de industrias poco higiénicas y en superficies de alimentos no cocidos,
a 8 en suelos de restaurantes, cocinas, habitaciones de hospitales, baños,
a 4 en retretes
y a 1 en guarderías, lavabos, mesas de hospitales, superficies de catering y lavandería…
De todas formas y, en general, nada mejor que la propia experiencia en su fábrica y su producto para saber cuando los valores se disparan de forma alarmante.
Por ello es tan interesante el uso rutinario de DESINFECTEST®.
3.‑ Para identificación de colonias:
No se efectúa recuento.
El medio selectivo en el que haya crecimiento será indicador del tipo de microorganismos de que se trata.
Debe confirmarse, antes de emitir un diagnóstico, con kits específicos adecuados, sean bioquímicos o sean inmunológicos (consultar al Servicio Técnico de MICROKIT).
NOTA: Si la presencia de microorganismos es muy abundante, se puede obtener un crecimiento uniforme, formándose un velo que puede pasar desapercibido;
en tal caso la superficie pierde su brillo.
Para estos casos, debe analizarse de nuevo la muestra tras diluirla a razón de 0,1 g (o ml) en 100 ml de Agua Peptonada Tamponada estéril (MICROKIT RPL007),
y después multiplicar el resultado obtenido por 1.000.
A veces no aparecen colonias en el medio de cultivo, y sí entre éste y el plástico soporte.
En tal caso, debe repetirse el análisis, pues es señal de que no se dejó gotear bien el líquido sobrante tras la inmersión.
Algunos medios viran al color típico de las colonias cuando la concentración de éstas es tan alta que no se distinguen; así, su presencia no pasa desapercibida.
PRECAUCIONES
- Leer bien las instrucciones para cada tipo de laminocultivo.
- No tocar las láminas agarizadas.
- No abrir más que en el momento de uso, para conservar la esterilidad.
- Evite utilizar más que una sola vez cada laminocultivo.
- Desechar los laminocultivos que, ocasionalmente, aparezcan contaminados, deslaminados, retraídos, caducados o secos.
- Evitar los cambios de temperatura para que no aparezca agua de condensación y para que el agar no pierda convexidad. No congelar. Mantener a una temperatura ambiente comprendida entre 4 y 25 ºC, pero sin cambios diurnos/nocturnos importantes, lejos de las corriente de aire y de la luz (sobre todo el Agar Rosa Bengala).
- Destruir los laminocultivos usados mediante incineración, inmersión prolongada en desinfectantes (lejía, alcohol …) o autoclavado.
- Use cepas de referencia CRIOSTRAINS, de trabajo o cuantitativas, para validar los reactivos una vez llegados a fábrica o tras almacenamientos prolongados o inadecuados.
CADUCIDAD
La caducidad de los laminocultivos es de 6 meses desde fabricación (Cad. mínima de venta 2 meses).
No obstante, puede prolongarse hasta 3 meses después de la fecha de caducidad impresa en la caja, si se mantienen en nevera a 8-12 ºC, sin variación de temperatura
y siempre que los agares mantengan su convexidad por encima del reborde de plástico de la lámina.
LA GAMA MAS COMPLETA DE LAMINOCULTIVOS: DESINFECTEST ®

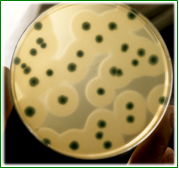
DESINFECTEST®-AEM/ AET: Recuento total, con inactivadores, de bacterias aerobias mesófilas y totales:
Este índice es indicador de higiene. Cuanto mayor sea el recuento, más rápidamente se degradará el producto.
Ambas caras tienen Agar Neutralizing sin púrpura y con TTC.
Bacillus subtilis crece con amplias colonias rugosas,
Escherichia coli crece con colonias húmedas y cremosas,
Pseudomonas aeruginosa crece con colonias incoloras y
Staphylococcus aureus crece con colonias amarillas.
Otros muchos microorganismos crecen con colonias más o menos características.
El TTC tiñe las colonias de rojo, permitiendo una clara diferenciación respecto al fondo.
Si toda la cara se tiñe de rosado, es que el recuento es tan alto que las colonias compiten por el sustrato hasta el punto de ser diminutas y no verse.
El Neutralizing inactiva los residuos de derivados de amonio cuaternario, fenoles, formoles, iodo, cloro, mercurio, glutaraldehido… que pueda haber en la muestra o superficie.
Este laminocultivo se incuba a 35‑37 ºC durante 24‑72 horas.
Se leen todas las colonias (ver tabla de resultados superior).
Se obtiene el recuento total de aerobios mesófilos incluidos los de crecimiento lento y los subletales tras las desinfecciones.
DESINFECTEST®-MIX: Recuento total de hongos (levaduras y mohos) saprófitos-ambientales, alterativos y parásitos-patógenos:
Los hongos saprófitos, alterativos o ambientales son un índice indicador de higiene. Cuanto mayor sea el recuento, mas rápidamente se degradará el producto.
La cara rosa contiene Agar Rosa de Bengala con cloranfenicol, medio de color rosado especial para el crecimiento selectivo de hongos (levaduras y mohos) ambientales.
La presencia de Rosa de Bengala restringe el tamaño de los mohos, impidiendo que los de crecimiento rápido invadan la superficie del medio, oculten a los más lentos e impidan el recuento.
El cloranfenicol (CAF), antibacteriano de amplio espectro, proporciona una gran selectividad para los hongos.
Este medio es sensible a la luz, por lo que la preocupación general de guardar los laminocultivos en sus cajas y lejos de la luz se acentúa aquí.
También la incubación, para este medio, debería hacerse en la oscuridad.
La recuperación selectiva de levaduras y mohos en este medio es máxima, según demuestra un estudio comparativo de MICROKIT: Sanchis & Co. Técnicas de Laboratorio, Mayo de 1996.
La cara incolora es Neutralizing Agar incoloro y con TTC para recuento total (como en AEM)
Este laminocultivo se incuba, para hongos ambientales, a 21-35 ºC durante 3-5 días.
En general, a los tres días aparecen las levaduras y algunos mohos de crecimiento rápido, y a los 5 días aparecen todos los mohos
Se leen todas las colonias (ver tabla de resultados inferior).
Las colonias de levaduras aparecen con el mismo aspecto que la mayoría de bacterias, y también con colores diversos.
Los mohos producen colonias filamentosas (no confundir con las colonias en «melena de león» de algunos Bacillus), pulverulentas y de colores diversos.
Candida albicans aparece en ambas caras con colonias exuberantes y blancas o rosadas. Confirmar la especie con galerías de identificación para levaduras (MICROKIT YEAST-IDENT).
Aspergillus niger y Rhizopus nigricans crecen en ambas caras con colonias filamentosas blancas o amarillas, que ennegrecen centrífugamente en unos días por formación de esporas.
Aspergillus flavus, aflatoxigénico, crece en ambas caras con colonias filamentosas amarillas.
Muchas especies de Alternaria crecen en ambas caras con colonias teñidas de marrón oscuro a causa de sus esporas.
Muchas especies de Penicillium y de Aspergillus crecen en ambas caras con colonias verdes, amarillas y azuladas a causa de sus esporas.
Las identificaciones de mohos deben hacerse con la ayuda de un microscopio y claves dicotómicas (MICROKIT regala unas si las solicita junto a su pedido).
Este laminocultivo se incuba, para bacterias ambientales (saprófitas), 1-3 días a temperatura ambiente (21-25 ºC). Todas las colonias crecerán rojas.
Para bacterias patógenas y/o asociadas al hombre, se incuba a 35-37ºC,
pero en este caso la cara de hongos sólo permitirá el crecimiento de hongos (levaduras y mohos) patógenos y oportunistas capaces de crecer a la temperatura de los animales de sangre caliente.
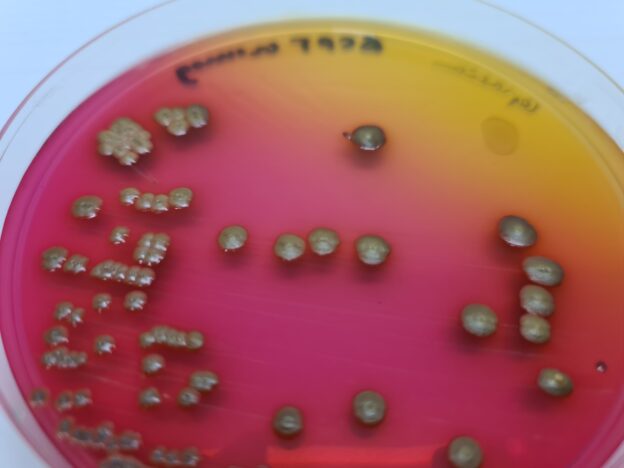
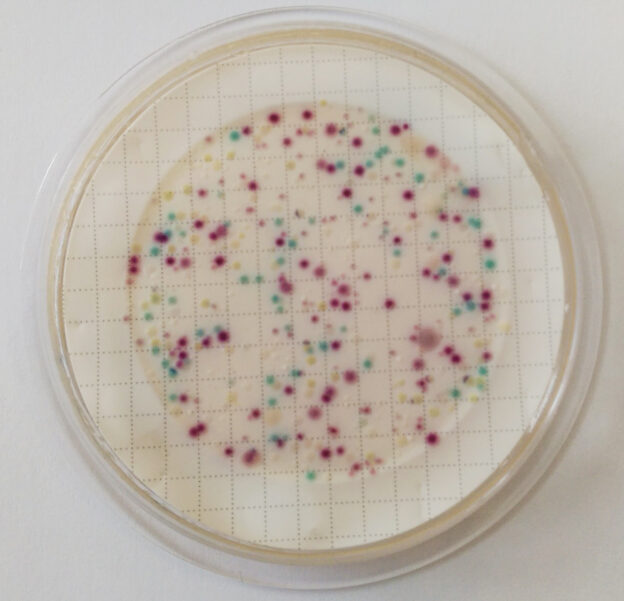
DESINFECTEST®-EC: Detección y recuento de Coliformes, Escherichia coli y Salmonella:
Los índices Coliformes y E. coli son diferentes indicadores de contaminación fecal por falta de higiene de las materias primas, los operarios, las aguas…
La aparición de Salmonella es extraordinariamente grave, pues es un serio patógeno que produce en nuestro país cerca de la mitad de las toxiinfecciones alimentarias.
Una cara contiene Agar cromogénico Magenta-Gal para Salmonella.
La búsqueda de Salmonella en superficies puede realizarse con este laminocultivo.
Sin embargo, su búsqueda en productos requiere, además, un pre-enriquecimiento revitalizador (Agua Peptonada Tamponada Neutralizante estéril MICROKIT)
y un postenriquecimiento multiplicador y selectivo (Caldo Rappaport estéril MICROKIT o mucho mejor, caldo SS MICROKIT).
La otra cara contiene Agar Cromogénico MugPlus (CCA) para E.coli y demás coliformes.
Este laminocultivo se incuba a 35-37 ºC durante 24 (-48) horas.
Salmonella crece en la cara de Agar cromogénico para Salmonella con colonias rojas o verdes.
Otras enterobacterias pueden crecer, pero lo suelen hacer con otros colores.
Confirmar sólo las colonias sospechosas, con KITS bioquímicos o inmunológicos de MICROKIT.
En la otra cara, las colonias púrpuras, rosas, rojizas o violáceas son de Coliformes
y las colonias azules, violetas o turquesa que resultan indol positivas (Indol Kovacs SBH056, el reactivo vira de amarillo a rosa), son E.coli.
Como E.coli tambien es coliforme, en el recuento de coliformes se suman todas las colonias rojizas y azules.
DESINFECTEST®-ARICPC:
Una cara con Neutralizing Agar incoloro +TTC para recuento total (Ver AEM)
Otra cara con VRBG Agar + Inactivadores para recuento de Enterobacterias (colonias púrpura sobre medio púrpura)
SOLUCIONES A LAS LIMITACIONES DE LOS LAMINOCULTIVOS.
1.‑ Análisis cuantitativos
El sistema de laminocultivos o dipslides DESINFECTEST® es ideal para análisis de superficies, para análisis de campo, para laboratorios móviles y para pequeños laboratorios.
Sus resultados, excepto en el control de superficies, son semicuantitativos, por lo que también son ideales para muestras muy contaminadas.
Pero si se requieren resultados cuantitativos o si se analizan productos con baja contaminación deben utilizarse tubos preparados MICROKIT con 20 ml de Agar adecuado,
que se funden al Baño María y se añaden a 1 ml de la muestra vertida en una placa de Petri (Solicite catálogo de tubos MICROKIT).
Para realizar diluciones de la muestra se utilizarán tubos preparados MICROKIT con 9 ml del Caldo adecuado:
Solución RINGER (TPL109), Agua Peptonada Tamponada (TPL007), Agua de Triptona (TPL034), Agua destilada estéril (TPL001) o LPT100 Neutralizing Broth (TPL023).
2.‑ Anaerobios
Los laminocultivos están pensados para la detección de microorganismos aerobios. Para anaerobios pueden utilizarse otras técnicas:
Anaerobios en general: Tubos parafinados con 9 ml de Agar Schaedler (TPL193) que se inoculan fundiendo el medio y añadiendo la muestra, volteando el tubo sin agitar y dejándolo solidificar en posición vertical.
Sulfito‑Reductores (Clostridios…): Tubos parafinados con 9 ml de Agar SPS (TPL049) o frascos parafinados con 50 ml de SPS a doble concentración (RPL062) que se inoculan como los anteriores.
Anaerobios Reductores del Sulfato (Desulfovibrio…): Tubos con 9 ml de Sulfate American Petroleum Institute Agar con capilar de inoculación (TPL048).
De todas formas, nada nos impide hacer un recuento de anaerobios con DESINFECTEST®-AEM/AET incubado, con el tapón sin apretar, en anaerobiosis
(Bolsas de anaerobiosis KKM038 o generadores de atmósfera anaeróbica en jarra KKM036, e indicador de anaerobiosis KKM039).
En tal caso, tomar la precaución de realizar un duplicado para los anaerobios esporulados, e incubar este segundo laminocultivo tras someterlo a un shock térmico a 65 ºC durante 3 horas,
a fin de que germinen las esporas que de otra manera darían resultados falsamente negativos.
NOTAS FINALES SOBRE MUESTREO E INTERPRETACION DE RESULTADOS EN SUPERFICIES:
Después de evaluar el grado de contaminación ambiental, es necesario tener en cuenta los límites de aceptabilidad, que no pueden darse como norma general ya que no son comparables una sala estéril de un laboratorio farmacéutico con un almacén de cítricos, por ejemplo.
Dichos limites deben ser fijados en función de las investigaciones propias, estudiando la correlación existente entre el nivel de la contaminación ambiental y el de la contaminación del producto, en el caso de la industria.
La investigación se hará siempre inmediatamente antes e inmediatamente después de la desinfección ambiental y, al menos, durante el primer mes (en Laboratorios Farmacéuticos, siempre), a diario.
Posteriormente la frecuencia mínima será semanal.
Un recuento similar antes y después de la desinfección, es indicador de que el desinfectante elegido no es el adecuado.
Ya que las mismas personas estamos continuamente contaminándolo todo.
Recuentos ascendentes a lo largo de unos días seguidos, son indicadores de que ha llegado el momento de desinfectar de nuevo o de alternar el desinfectante.
Estudios internos inéditos demuestran que la distribución de microorganismos en superficies de ambientes humanos no es homogénea, sino heterogénea
(contagiosa: muchas células junto a micropartículas de materia orgánica y pocas en grandes huecos).
Por ello recomendamos una muestra mínima de 100 cm2 (10 caras de laminocultivo), que sí resulta representativa de la realidad.
Otro estudio interno, también inédito, demuestra que el medio sólido por contacto no toma el 100 % de la población de la superficie;
depende de la naturaleza de la superficie y de la tensión superficial del medio (su hidratación y su composición).
Al hacer un segundo contacto en la misma superficie exacta se vuelven a obtener recuentos de hasta un 40% con respecto a la primera toma
y en un tercer contacto de hasta un 10% con respecto a la primera toma.
Por ello, recomendamos segundas tomas en la misma superficie para obtener resultados más cercanos a la realidad.
Límites de aceptabilidad APHA
Para el recuento total, puede tenerse en cuenta la escala proporcionada por el Comite of Microbial Contamination of Surfaces of the Laboratory Section of the A.P.H.A. (Tras la desinfección):
LUGAR NUMERO DE COLONIAS POR 25 cm2
BUENO REGULAR MALO
Suelo habitación hospital 0‑25 26‑50 más
Mesa habitación hospital 0‑5 6‑15 más
Guardería 0‑5 6‑15 más
Suelo baño 0‑25 26‑50 más
Retrete baño 0‑15 16‑25 más
Tocador baño 0‑5 6‑15 más
Otros límites de aceptabilidad
En catering, Solberg and Co. (Food Technology 12‑1990) recomiendan recuentos inferiores a 1 colonia por 25 cm2 en productos recién lavados y a 4 colonias por 25 cm2 (3 caras de DESINFECTEST®) en productos lavados hace dos semanas.
En Laboratorios Farmacéuticos, no es bueno obtener recuentos superiores a 5 UFC por 25 cm2-3 caras de DESINFECTEST®- (En zona estéril, el recuento deberá ser de 0).
Y en Superficies de fábricas de productos cárnicos, Niskanen and Pohja (1977) recomiendan un máximo de 480 cfu, de 25 Escherichia coli y de 25 Staphylococcus aureus por cada muestra de 25 cm2 (3 caras de DESINFECTEST®).
Límites de aceptabilidad ISO 100012
Por fin una Norma ISO termina con este caos de valores de aceptabilidad (UNE-EN-ISO 100.012), permitiendo que haya menos de 100 ufc/25 cm2 de bacterias
y menos de 100 ufc/25 cm2 de hongos antes de la desinfección/limpieza;
y que haya menos de 10 ufc/25 cm2 de bacterias y menos de 10 ufc/25 cm2 de hongos tras la limpieza o desinfección.
Dado que un laminocultivo DESINFECTEST® tiene una superficie de 10 cm2, debe haber menos de 40 colonias de bacterias o de hongos por cara antes de la desinfección/limpieza
y menos de 4 colonias de bacterias o de hongos por cara tras la desinfección/limpieza.
Ideal para ello resulta el DESINFECTEST®-MIX.
Lugares de muestreo
Es fundamental la elección de los puntos críticos de muestreo más representativos para controlar en ellos la higiene de forma rutinaria y realizar, así, las desinfecciones en el momento oportuno, ni antes ni después.
‑ Industria alimentaria:
Zonas de procesado, equipos, cintas transportadoras, superficies de trabajo, salas de despiece, máquinas de escaldado, zonas de empaquetado…
…tanques de procesado, almacén de materias primas, almacén de producto terminado, manos y ropa de los manipuladores…
…suelos de oficinas, Laboratorio de Control Microbiológico, aparatos de aire acondicionado, W.C…
‑ Laboratorios de Control Microbiológico:
Cabina de flujo laminar, superficies de manipulación microbiológica, estufas de cultivo…
…nevera, suelos, ropa y manos de los operarios, W.C…
‑ Hospitales:
quirófanos (incluidos mesa de operaciones y utensilios), habitaciones de enfermos, salas de maternidad, U.C.Is…
…salas de consulta, salas de espera, lavandería, cocina, aparatos de aire acondicionado, suelos de pasillos…
…W.C., laboratorios de bacteriología y micología…
‑ Otros lugares públicos:
Guarderías, escuelas, residencias de ancianos, cocinas, oficinas, restaurantes…
…habitaciones de hoteles, lavabos, transportes públicos…
El usuario final es el único responsable de la destrucción de los organismos que se hayan multiplicado, según la legislación medioambiental vigente. Autoclavar antes de desechar a la basura.
Destruir por inmersión en lejía. Mantener fuera del alcance de los niños. No ingerir.
Diseñado por LABORATORIOS MICROKIT, S.L. desde 1.989. Revisado en Octubre, 2016
DESINFECTEST ® es marca registrada de Laboratorios MICROKIT, S.L.
Si desea más información sobre nuestro DESINFECTEST – LAMINOCULTIVOS póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es
https://www.microkit.es/monograficos/6-Control-de-superficies-monograf–a.pdf
No se pierda el vídeo:
https://youtu.be/qJB0elPYvVU