BGBL 2% MUG BRILLIANT GREEN BILE LACTOSE BROTH MUG Detección y enumeración de E.coli y resto de coliformes por la técnica NMP.
COMPOSICIÓN
- Peptona 10,00 g
- Sales biliares 20,00 g
- Lactosa 10,00 g
- Triptófano 1,00 g
- MUG 0,10 g
- Verde brillante 0,01 g
(Fórmula por litro) pH final: 7,2 ± 0,1 ![]()
PARA USO EXCLUSIVO EN LABORATORIO. MANTENGA EL BOTE BIEN CERRADO EN LUGAR SECO, FRESCO Y OSCURO. AGITE EL BOTE ANTES DE USAR.
PREPARACIÓN
Disolver 41 gramos de medio en 1 litro de agua bidestilada. Dispensar en tubos con campana Durham. Autoclavar a 121 ºC durante 15 minutos. No sobrecalentar ni recalentar.
NOTA: No debe sobrepasarse el tiempo de autoclave ni volver a recalentar el medio.
PRECAUCIÓN: CONTIENE SALES BILIARES.
DESHIDRATADO CODIGO: DMT026
CONTROL DE CALIDAD DEL MEDIO
Realizado en nuestro laboratorio; es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio, tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…)
DESHIDRATADO: Polvo fino, verdoso
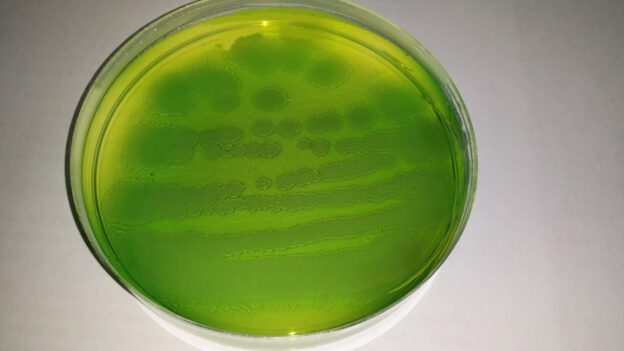
PREPARADO: Estéril, Verde esmeralda
CONTROL DE CRECIMIENTO CUANTITATIVO 24-48 h a 37°C aprox:
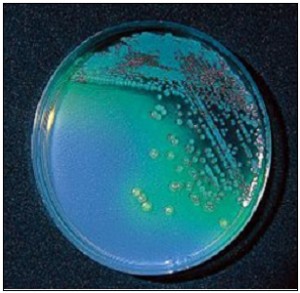
- Escherichia coli MKTA 25922, 9 tubos forman gas y son fluorescentes bajo 366 nm, a 37° y a 44°C.
- Salmonella abony MKTN 6017, 9 tubos sin gas ni fluorescencia.
- Enterococcus faecalis MKTA 29212, Inhibido.
- Klebsiella oxytoca MKTA 13182, 9 tubos con gas, no fluorescentes, sólo a 37°C.
PRESENTACIÓN: MEDIO DESHIDRATADO
NOTA: El compuesto fluorogénico MUG añadido al medio BGBL 2% permite la detección y recuento (NMP) de E. coli de forma rápida y sin necesidad de incubación a 44,5 ºC.
SIEMBRA
Inocular cada tubo con 1 ml de muestra y su serie de diluciones decimales (en NMP, 15 tubos por muestra). Incubar 24-48 horas a 35 ºC aproximadamente.
INTERPRETACIÓN
La acidificación (viraje a amarillo en los casos más extremos) con producción de gas (retenido en la campana Durham) es prueba positiva para coliformes. Además, la emisión de luz azul bajo 366 nm (linterna MICROKIT) indica presuntos E.coli, confirmables con indol Kovacs (SBH056): anillo rojo, positivo.
Si desea más información sobre nuestros MEDIO BRILLIANT GREEN BILE BROTH 2% LACTOSE MUG rellene nuestro formulario de contacto http://www.medioscultivo.com/contacto . O si lo prefiere póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16
https://www.microkit.es/fichas/BRILLIANT-GREEN-BILE-BROTH-MUG.pdf