Bacillus anthracis selective Agar
o Antrax Agar es el medio selectivo para aislar este patógeno y sus esporas, selectivo para la detección y recuento de Bacillus anthracis en todo tipo de muestras (lana, tierra, superficies, aire, heridas…).
COMPOSICIÓN
- Infusión de corazón 17,5 g
- Peptona pancreát.gelatina 10,0 g
- Triptosa 10,0 g
- Extracto de levadura 1,5 g
- Cloruro sódico 5,0 g
- Glucosa 10,0 g
- Agar-Agar 14,0 g
pH final: 7,3 ± 0,2
En suplemento pinchable aparte:
- Factor Lz 40 mg
- Polimixina B 30.000 UI
PREPARACIÓN
Disolver 68 gramos en 1 litro de agua bidestilada. Agitar calentando hasta ebullición. Autoclavar a 121° C durante 15 minutos. El color final del medio es crema. No sobrecalentar. Enfriar a 47°C y añadir asépticamente 20 ml del suplemento selectivo para Bacillus anthracis SMT008 (Polimixina B + Factor Lz). Agitar hasta su completa solidificación para evitar grumos.
PARA USO EXCLUSIVO EN LABORATORIO. AGITE EL BOTE ANTES DE USAR. MANTENGA EL BOTE BIEN CERRADO EN LUGAR SECO, FRESCO Y OSCURO.
DESHIDRATADO CODIGO: DMT018
CONTROL DE CALIDAD DEL MEDIO:
Realizado en nuestro laboratorio; es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio, tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…).
DESHIDRATADO: Polvo grueso, Crema PREPARADO: Estéril, Crema
CONTROL DE CRECIMIENTO 48-72 h a 37°C aproximadamente, o bien 3-5 días a temperatura ambiente (21-28°C aproximadamente):
Bacillus anthracis MKTA 23445, Excelente.
Staphylococcus aureus MKTA 6538P, Crece, pero tras 48 horas, colonias redondas y discretas.
Pseudomonas aeruginosa MKTA 27853, Inhibido.
Escherichia coli MKTA 25922, Inhibido.
PRESENTACIÓN:
MEDIO DESHIDRATADO. PLAQUITAS HERMÉTICAS PREPARADAS (PLAQUIS ®).
SIEMBRA E INTERPRETACIÓN
Para evitar interferencias o inhibición del crecimiento por parte de ciertos componentes de la muestra (residuos de desinfectantes u otros inhibidores, flora interferente…), para lana, tierra, sobres, etc. es preferible realizar la suspensión inicial (1:10) en LPT Neutralizing Broth (deshidratado DMT217, frascos 90 ml RPL054) y dejar actuar 20-30 minutos.
Sembrar en superficie 0,1-0,3 ml de la suspensión inicial de la muestra y su serie de diluciones decimales.
Si se trata de controlar superficies, aplicar la placa de contacto durante 10 segundos, apretando sin restregar.
Si se analiza el aire, tomar 5 muestras de 200 litros cada una con muestreador de impacto con placa de contacto (MICROFLOW VAQ055) a fin de minimizar el efecto desecación y el efecto rebote, respectivamente.
Incubar 8-24 horas a 35 °C aprox.
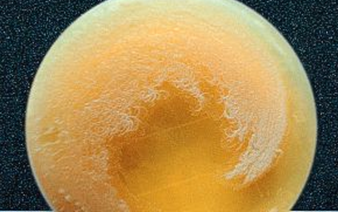
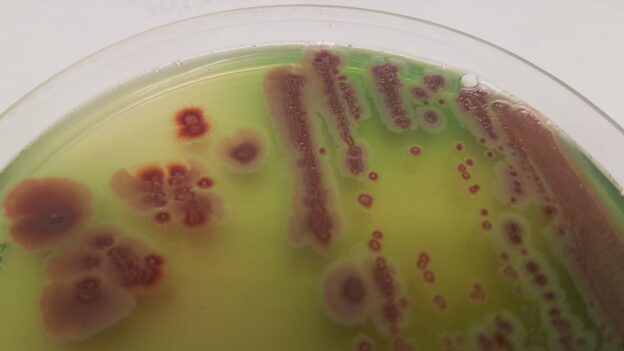
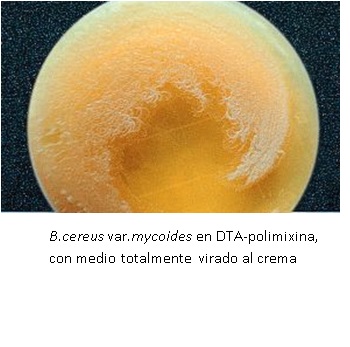
B.anthracis crece con colonias grandes, a veces lobuladas.
Al microscopio se ven cadenas cortas de 2-4 bacilos Gram positivos con espora redonda, central, que no deforma la pared celular. La esporulación se ve inhibida con altas concentraciones de CO2, como las que hay en el interior del huésped.
Las cepas patógenas poseen una gran cápsula que se evidencia al teñir con tinta india.
NOTA:
Bacillus anthracis fué la primera bacteria detectada como patógena, en 1877 por Robert Kock.
La palabra antrax viene del griego, carbón, a causa de la lesión negra que provoca en la piel del ganado y el hombre.
La enfermedad se llama carbunco y es una zoonosis transmitida por herbívoros infectados a humanos expuestos, como los pastores, veterinarios…
Es frecuente en suelos alcalinos y de ahi pasa a la lana, piensos, etc.
Existen al menos 89 cepas conocidas, algunas altamente virulentas (como las empleadas en la guerra bacteriológica y terrorismo) y otras benignas, las cuales siempre carecen de cápsula.
La virulencia depende de la posesión de ciertos genes que producen un polipéptido capsular antifagocitario (substancia P, generada por el plásmido pX02) y una exotoxina (generada por el plásmido pX01).
Su diferenciación bioquímica de otras especies (B.cereus, B.coagulans, B.mycoides y B.thuringiensis) es imposible (todas ellas pueden crecer en agar anaerobio, a pH 5,7 y no acidifican la arabinosa) por lo que es probable que se trate de distintas formas de una misma especie.
Si desea más información sobre nuestros MEDIO BACILLUS ANTHRACIS SELECTIVE AGAR rellene nuestro formulario de contacto http://www.medioscultivo.com/contacto .
O si lo prefiere póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16
https://www.microkit.es/fichas/BACILLUS-ANTHRACIS-SELECTIVE-AGAR.pdf
https://www.microkit.es/monograficos/10-Bacillus-monograf–a.pdf