CEREBRO CORAZÓN BRAIN HEART INFUSION AGAR. Detección de microorganismos difíciles y de la estafilocoagulasa.
COMPOSICIÓN
- Extracto corazón‑cerebro 17,5 g
- Peptona pancreát.gelatina 10,0 g
- Cloruro sódico 5,0 g
- Fosfato disódico 2,5 g
- Glucosa 2,0 g
- Agar-Agar 10,0 g
(Fórmula por litro)
pH final : 7,1 ± 0,2
MATERIAL PROCEDENTE EXCLUSIVAMENTE DE CERDO
PREPARACIÓN
Disolver 47 gramos de medio en 1 litro de agua bidestilada. Calentar hasta ebullición, agitando, para su total homogeneización. Repartir en tubos o frascos y esterilizar en autoclave a 121 ºC durante 15 minutos. No sobrecalentar, para evitar el oscurecimiento y caramelización del medio.
PARA USO EXCLUSIVO EN LABORATORIO MANTENGA EL BOTE BIEN CERRADO EN LUGAR SECO, FRESCO Y OSCURO. AGITE EL BOTE ANTES DE USAR.
DESHIDRATADO CODIGO: DMT021
CONTROL DE CALIDAD DEL MEDIO
Realizado en nuestro laboratorio; es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio, tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…)
DESHIDRATADO: Polvo fino, Tostado
PREPARADO: Estéril, Ambar precipitado
CONTROL DE CRECIMIENTO 24-48 h a 37°C aproximadamente:
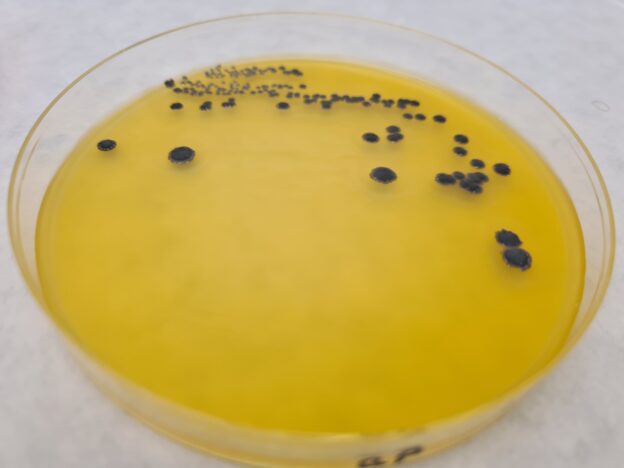
- Aspergillus niger MKTA 16404, Excelente, colonias algodonosas, amarillas, discretas. Con respecto a PCA estandarizado*, recuento medio 81 %.
- Candida albicans MKTA 10231, Excelente, redondas, bien desarrolladas. Con respecto a PCA estandarizado*, recuento medio 99 %.
- Bacillus subtilis MKTA 6633, Excelente, colonias expandidas, discretas. Con respecto a PCA estandarizado*, recuento medio 118 %.
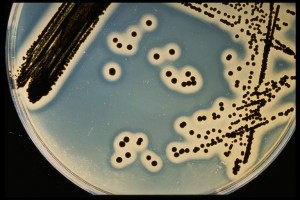
- Staphylococcus aureus MKTA 6538P, Excelente, colonias redondas, discretas. Con respecto a PCA estandarizado*, recuento medio 102 %.
- Pseudomonas aeruginosa MKTA 9027, Excelente, colonias grandes, lenticulares, pigmentadas. Con respecto a PCA estandarizado*, recuento medio 177 %.
- Escherichia coli MKTA 25922, Excelente, colonias grandes, lenticulares. Con respecto a PCA estandarizado*, recuento medio 90 %.
* El que cumple con recuperación superior al 92-125% con respecto a cepas cuantitativas trazables a cepa tipo.
PRESENTACIÓN: FRASCOS PREPARADOS, MEDIO DESHIDRATADO
MODO DE EMPLEO E INTERPRETACIÓN DE RESULTADOS
Inocular en superficie 0,1 ml de muestra o de caldo BHI. Incubar el tiempo y a la temperatura óptimos para el microorganismo que se desea aislar (a falta de otro criterio, 24-72 horas a 35-37 ºC aproximadamente). Dada la riqueza de sus componentes, la recuperación (tanto de recuento total como de patógenos) es superior a la de otros medios generales
Si desea más información sobre nuestros MEDIO BRAIN HEART INFUSION AGAR, rellene nuestro formulario de contacto http://www.medioscultivo.com/contacto . O si lo prefiere póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16
https://www.microkit.es/fichas/BRAIN-HEART-INFUSION-AGAR.pdf






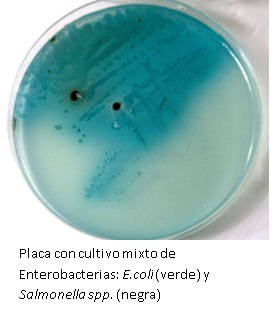




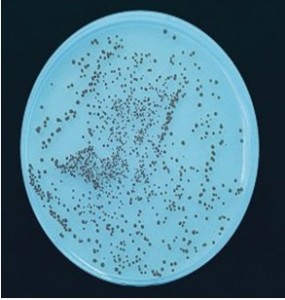
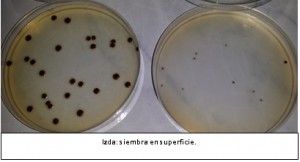 Izda: siembra en superficie; Dcha: siembra en masa, mucho menos eficiente para este microorganismo
Izda: siembra en superficie; Dcha: siembra en masa, mucho menos eficiente para este microorganismo