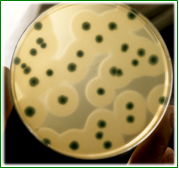
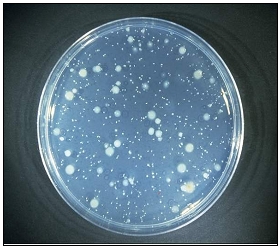
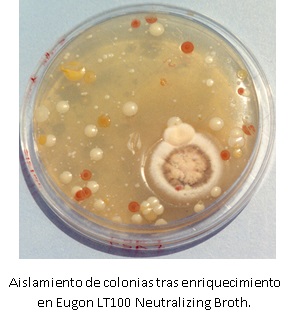
Mac CONKEY SORBITOL AGAR es el medio de cultivo clásico para la detección y recuento de la variante O157 de E.coli
Detección presuntiva de E.coli serovar. O157 (UNE-EN ISO 16654:2002) a partir de alimentos (carne de vacuno,…), aguas y otras muestras, previamente enriquecidas en E. coli O157 Broth.
COMPOSICIÓN
- Peptona de caseina 17,00 g
- Peptona de carne 3,00 g
- D Sorbitol 10,00 g
- Sales Biliares 1,50 g
- Cloruro sódico 5,00 g
- Rojo Neutro 0,030 g
- Cristal violeta 0,001 g
- Agar agar 12,00 g
(Fórmula por litro) pH final 7,1 ± 0,2
PARA USO EXCLUSIVO EN LABORATORIO.
AGITE EL BOTE ANTES DE USAR.
MANTENGA EL BOTE BIEN CERRADO, EN LUGAR SECO, FRESCO Y OSCURO.
PRESENTACIÓN: MEDIO DESHIDRATADO
CÓDIGO: BCD161
PREPARACIÓN
Disolver 48.5 gramos en 1 litro de agua bidestilada.
Calentar, agitando hasta ebullición, para su total disolución.
Autoclavar a 121 ºC durante 15 minutos.
No sobrecalentar.
Añadir a 44-47 ºC, 20 ml de Telurito-Cefixime estéril (BCX161) (= 2’55 mg/l) y mezclar.
CONTROL DE CALIDAD DEL MEDIO
Realizado en nuestro laboratorio; es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio, tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…)
DESHIDRATADO: Polvo fino, púrpura
PREPARADO: Violáceo
EVALUACIÓN DEL RENDIMIENTO ISO/TS 11133-2 18-24 h a 37 ºC, aplicando el método ISO 16654 o el indicado en el Manual MICROKIT actual:
- E.coli (0157:H7) MKTA 35150, Excelente, colonias amarillentas o suavemente rosadas y 1 mm de diámetro. PR >50% de colonias respecto al número de ufc certificadas e inoculadas en TSA; la variabilidad de la productividad depende de la composición y carga de la flora acompañante inoculada.
- E. coli MKTA 25922, Excelente, pero con colonias rosa-púrpura
- Staphylococcus aureus MKTA 6538, totalmente inhibido
Las colecciones TIPO prohiben el uso de su referencia por lo que indicamos la nuestra, directamente trazable a la colección TIPO.
MODO DE EMPLEO
Tras enriquecer en caldo O157 m-TSB (BCD165), no más de 18-24 h a 41,5°C aproximadamente: Inocular en superficie muestra y diluciones para obtener muchas colonias bien aisladas.
Incubar a 37 ºC aproximadamente durante no más de18-24 horas.
INTERPRETACIÓN DE RESULTADOS
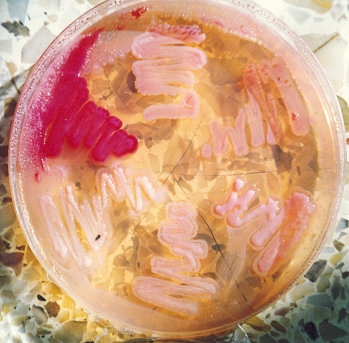
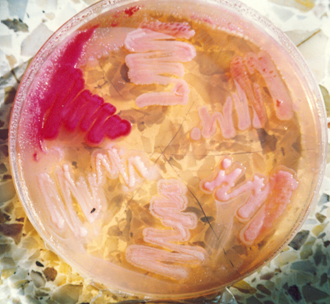
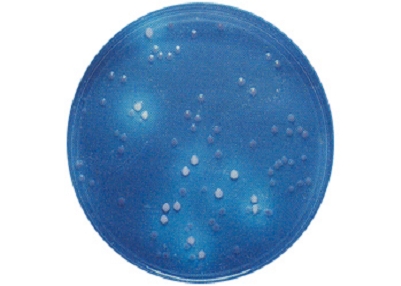
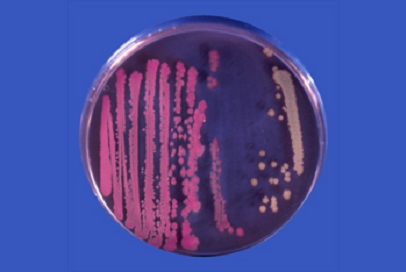
E. coli enterohemorrágico, serovariedad O157 H7 crece con colonias casi incoloras, rosa pálido-amarillentas, al no fermentar el sorbitol, de 1 mm de diámetro.
Otras cepas de E. coli crecen con colonias púrpuras.
Resembrar colonias bien aisladas en Agar Nutritivo para E.coli O157 (DMT126).
Incubar 18 h a 37°C aproximadamente.
Si se prolonga la incubación, la distinción de colonias será más difícil.
Confirmar con los tests adecuados:
Indol en Agua de triptona con triptófano (BCD129), 24 h a 37°C aproximadamente y adición de Kovacs (SBH056),
látex O157 y H7 ,
controlando con cepa + y -.
Según un método bastante difundido, si se añaden 0’1 g/l de MUG (SKL061) en el medio antes de autoclavar, las colonias de E. coli O157 H7 son las NO fluorescentes bajo luz de 366 nm (VMT050).
El usuario final es el único responsable de la destrucción de los organismos que se hayan desarrollado, según la legislación medioambiental vigente. Autoclavar antes de desechar a la basura.
Si desea más información sobre nuestros Mac CONKEY SORBITOL AGAR, rellene nuestro formulario de contacto http://www.medioscultivo.com/contacto . O si lo prefiere póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16
https://www.microkit.es/fichas/Mac-CONKEY-SORBITOL-O157-AGAR.pdf


 PRECAUCIÓN: CONTIENE SALES BILIARES.
PRECAUCIÓN: CONTIENE SALES BILIARES.