LEGIONELLA AGAR (BCYE , BCYE -Cys, GVPC…) son los medios de cultivo estándar para la detección y recuento de Legionella
Aislamiento selectivo de Legionella por el método MF o por siembra directa (ISO 11731:1998, ISO 11731-2:2004)
COMPOSICIÓN
Medio BASE (BCYE-Cys):
- Carbón activado 2,0 g
- Extracto de levadura 10,0 g
- Agar Agar 22,0 g
- Alfa-ketoglutarato (sal mono-K) * 1,0 g
- (Fórmula por litro)
- pH final: 6,9 ± 0,1
GVPC Suplemento Selectivo+Nutritivo estéril en solución 200 ml SBL604
Agite contundentemente y añada en asepsia 40 ml a 500 ml de medio enfriado a 50 ºC (o bien 8 ml a 100 ml de medio).
Puede contener precipitados por su elevada concentración pero desaparecen al diluir en el medio BCYE base. c.s.p. 2’5 l de medio.
Contiene las proporciones precisas, según ISO 11731, de: Tampón ACES, -Cetoglutarato, KOH, Clorhidrato de L-Cisteina, Pirofosfato férrico, Vancomicina, Cicloheximida, Polimixina y Glicina.
Contiene elementos tóxicos, evitar el contacto con la piel.
NOTA 1: La ref. SBL605 es idéntica al suplemento GVPC pero sin la Cisteína.
NOTA 2: EL caldo GVPC para preenriquecimiento revitalizador, es idéntico al Agar GVPC pero sin Agar-Agar y con el carbón granulado (ver kit P/A Legionella en tubos preparados, ref.RPL330). Ideal para usar antes de la ISO 11731 y encontrar de forma mucho más sensible y exacta la Legionella.
PREPARACIÓN (conversión del medio deshidratado en medio preparado)
Disolver 17 gramos de medio en 500 ml de agua bidestilada.
Calentar hasta hervir para la total disolución.
utoclavar a 121 ºC, 15 minutos.
El color final del medio es negro.
Enfriar a 45-50 ºC y, para el medio selectivo GVPC, añadir asépticamente 40 ml de Legionella Supplement-200 ml (SBL604, tampón ACES/KOH; nutritivo con -ketoglutarato, clorhidrato de L-cisteina y pirofosfato férrico; y selectivo, con Vancomicina, Polimixina, Cicloheximida y Glicina) ;
para el medio BCYE-Cys, añadir 40 ml de Legionella-Cys Supplement-200 ml (SBL605, tampón ACES/KOH, -ketoglutarato y pirofosfato férrico);
y para el medio BCYE, no son imprescindibles los antibióticos.
Mezclar muy bien y verter 20 ml/placa cuando el medio esté a punto de solidificar, para que la distribución del carbón activo sea lo más homogénea posible.
No sobrecalentar o el agar se volverá demasiado blando: Es posible que sea necesario añadir aún más Agar-agar (BCB006) para minimizar la friabilidad del agar, si se va a sembrar con asa (aceptado en ISO 11731).
PARA USO EXCLUSIVO
EN LABORATORIO.
MANTENGA EL BOTE BIEN CERRADO
EN LUGAR SECO, FRESCO Y OSCURO.
DESHIDRATADO CODIGO: DMT007
CONTROL DE CALIDAD DEL MEDIO
Realizado en nuestro laboratorio; es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio,
tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…)
DESHIDRATADO: Polvo, Negro
PREPARADO: Estéril, Negro.
CONTROL DE CRECIMIENTO 2 semanas a 37°C aproximadamente:
- Legionella pneumophila MKTN 12821 serogrupo1, Correcto, colonias gris-azuladas, cristalinas, mucosas, en 2-15 días, en medio suplementado BCYE+GVPC. No crece en medio BCYE base, sin suplemento nutritivo de hierro y cisteína. En el medio BCYE con suplemento nutritivo pero sin antibióticos, crece aproximadamente el doble de población que en el GVPC. Con respecto a PCA estandarizado y suplementado,* recuento 126 %, pero de forma selectiva.
- Legionella pneumophila serogrupo 2-15, MKTLeg-2, Idem.
- Escherichia coli, MKTA 25922 parcialmente inhibido. Con respecto a PCA estandarizado y suplementado,* recuento 27 %.
- Micrococcus luteus MKTA 9341, inhibido.
* El que cumple con recuperación superior al 92-125% con respecto a cepas cuantitativas trazables a la cepa tipo. Incertidumbres detectadas entre todos los lotes a lo largo de un año (la mayoría de la incertidumbre se debe a la cepa y a la proporción de cepas acompañantes inoculadas, no al medio).
PRESENTACION: MEDIO DESHIDRATADO (BCYE-BASE) Y SUPL. GVPC, KITS P/A caldo revitalizante, PLAQUIS HERMÉTICAS MF GVPC, FRASCOS PREPARADOS 100 ml (BCYE-BASE) + SUPL. GVPC.
MODO DE EMPLEO E INTERPRETACION DE RESULTADOS
Medio selectivo GVPC:
Inocular una membrana de filtración de 0’22 µm (VAC022, no usar de 0,45 µm), o mejor 0´1 ml de un extracto del fondo del tubo tras la centrifugación a 2500 r.p.m., 20′ de una muestra rascada, o bien 0’1 ml del fondo del caldo de enriquecimiento concentrado (RPL330) sobre una placa.
O aplicar una placa de contacto sobre la superficie, o bien introducirla en un aparato de control de aire.
Preincubar estrictamente 30 minutos a 50 ºC para eliminar la flora competitiva acompañante. Incubar a 35 ºC aproximadamente, en atmósfera húmeda de 2 a 14 días.
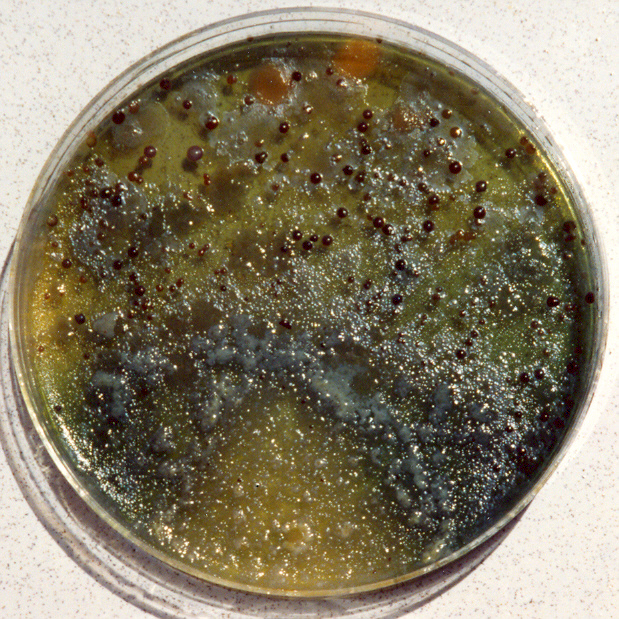
Las colonias de Legionella pneumophila son blanco-azuladas, brillantes, mucosas, de 1-2 mm Ø, circulares, lisas, algo elevadas y con los bordes enteros, fluorescentes en la oscuridad bajo luz UVA (linterna MICROKIT).
Subcultivar 3 colonias en BCYE (sin antibióticos) y en BCYE-Cys, al menos 2 días a 36 ± 1°C. Legionella crece en BCYE sin antibióticos (y en GVPC), pero no crece en BCYE-Cys (ni en medios generales tipo agar sangre, PCA, TSA, YEA, Nutrient Agar…).
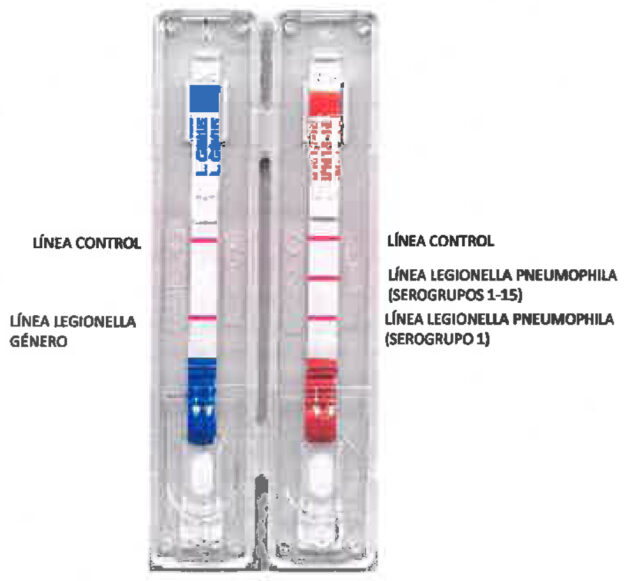
Las colonias deben confirmarse con oxidasa positivo, a menudo lento (KOT050), catalasa positiva (KMT299) y serotipado (M-IDENT-LEGIONELLA-VIRAPID MKTVR2, QUE PUEDE USARSE DIRECTAMENTE EN EL PRIMER AISLAMEINTO DE GVPC Y AHORRARSE ASÍ EL TIEMPO Y COSTE DE LAS OTRAS PLACAS DE BCYE y BCYE-Cys).
Contar sólo la placa de GVPC con más colonias de Legionella pneumophila. Si no se encuentra, expresar los resultados como “no detectada”, ya que a veces está presente y no crece. Peligro, microorganismos de alto riesgo para inmunodeprimidos, por inhalación de aerosoles (pero no llega a ser de Clase III).
El usuario final es el único responsable de la destrucción de los organismos que se hayan multiplicado, según la legislación medioambiental vigente. Autoclavar antes de desechar a la basura.
Si desea más información sobre nuestros MEDIOS LEGIONELLA BCYE AGAR, póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16
https://www.microkit.es/fichas/LEGIONELLA-GVPC-y-BCYE-AGAR-BASE.pdf
https://www.microkit.es/monograficos/9-Legionella-monograf–a.pdf