LETHEEN, EUGON O LPT NEUTRALIZING BROTH? Olvide ser esclavo de Normas ISO que no son de obligado cumplimiento, use lo mejor en cosméticos: LPT NEUTRALIZING BROTH
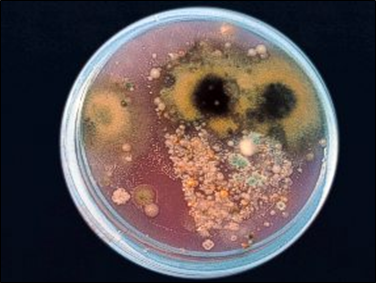
Caldo neutralizante y de enriquecimiento, con máxima recuperación. Emulsiona productos grasos y neutraliza TODO TIPO de conservantes. Ideal para cosméticos y desinfectantes. Con factores dopping para detectar tambien los hongos en menos tiempo (Candida albicans, Aspergillus spp…)
COMPOSICIÓN DE LA VERSIÓN LPT NEUTRALIZING BROTH SIN PÚRPURA
- Lecitina 1,40 g
- Triptona 20,00 g
- Extracto de levadura 10,00 g
- Cloruro Sódico 10,00 g
- Tioglicolato sódico 2,00 g
- Tiosulfato sódico 2,00 g
- Bi sulfito sódico 4,80 g
- Histidina 2,00 g
(Fórmula en g/l)
Ajustar a pH: 7,6 ± 0,2

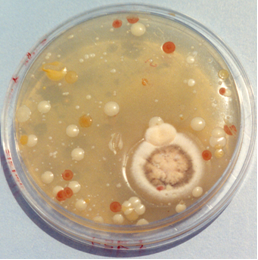
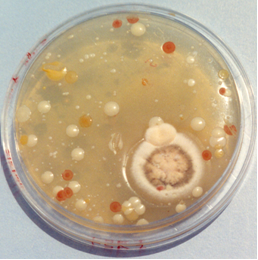
Izda: Sin inocular.
Dcha: Tubo turbio, con crecimiento a pesar de los conservantes
Este medio puede requerir hasta 15 ml de NaOH 1 N por cada litro de medio final
PREPARACIÓN
Disolver 26,1 g en alimentos y cosmética general (y a [x2], hasta 52,2 g en cosméticos muy inhibitorios, aunque el caldo quedará turbio) en 1 litro de agua bidestilada que contenga 5 ml de Polisorbato-Tween 80 atemperado.
Si se desea aumentar el poder neutralizante a mayor nivel que la [x2], debe añadirse a los 52,2 g/l, hasta un máximo de: 1,6 g/l de Lecitina, 30 ml/l de Polisorbato-Tween 80 y 5,4 g/l de Suplemento mix completo SMT002 (1 g/l de Histidina, 1 g/l de Tioglicolato Sódico, 2,4 g/l de Disulfito Sódico y 1 g/l de Tiosulfato Sódico).
Para inactivar además lactámicos, añadir penasa, para tetraciclinas añadir sales de Mg, para aminoglucósidos añadir heparina.
Agitar calentando hasta ebullición; en este medio la homogeneización puede requerir más tiempo del habitual.
Ajustar bien el pH final, ya que el Tween 80 acidifica incluso más de 1 punto, y en función de la calidad del agua empleada y de la proporción de polisorbato añadida, pueden requerirse hasta 15 ml de NaOH 1 N por cada litro de medio final.
Autoclavar 15 minutos a 121 ºC.
No sobrecalentar.
Una ligera turbidez es normal.
Los tubos y frascos con fondo denso son normales y deben homogeneizarse por agitación contundente justo antes de empezar los análisis.
Los frascos a [x2] (RPL054D) se preparan con 52,2 g/l de medio en polvo y 30 ml/l de Tween 80.
Otras combinaciones bajo pedido de al menos 180 u.
PARA USO EXCLUSIVO EN LABORATORIO. AGITE EL BOTE ANTES DE USAR. MANTENGA EL BOTE BIEN CERRADO EN LUGAR SECO, FRESCO Y OSCURO. DESHIDRATADO CODIGO: DMT217
CONTROL DE CALIDAD DEL MEDIO
Realizado en nuestro laboratorio; es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio, tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…)
DESHIDRATADO: Polvo grueso, Crema
PREPARADO: Estéril, Ámbar, con fondo precipitado. Artefactos: El fondo de los tubos preparados puede tener polisorbato precipitado: Agitar antes de usar.
EVALUACIÓN DEL RENDIMIENTO
s/ISO/TS 11133-2, 24-72 h a 35 ºC, aplicando el método indicado en el Manual MICROKIT actualizado:
- Escherichia coli MKTA 25922*, Excelente: Tras 25 minutos a 25°C, resiembra en TSA y obtención de >50-150% de colonias respecto al número de ufc inoculadas, en concreto 86-93%. Tras 24-48h, turbidez de ligera a elevada.
- Pseudomonas aeruginosa MKTA 9027*, Excelente: Tras 25 minutos a 25°C, resiembra en TSA y obtención de >50-150% de colonias respecto al número de ufc inoculadasm, en concreto 62%. Tras 24-48h, turbidez de ligera a elevada.
- Staphylococcus aureus MKTA 6538P*, Excelente: Tras 25 minutos a 25°C, resiembra en TSA y obtención de >50-150% de colonias respecto al número de ufc inoculadas, en concreto 51%. Tras 24-48h, turbidez de ligera a elevada.
- Candida albicans MKTA 10231*, Excelente: Tras 25 minutos a 25°C, resiembra en SDA y obtención de >50-150% de colonias respecto al número de ufc inoculadas, en concreto 66-104%. Tras 24-48h, turbidez de ligera a elevada.
- Burkholderia cepacia Colección TIPO USA 25416*, Excelente: Tras 20-30 minutos a 20-30°C, resiembra en TSA y obtención de >50-150% de colonias respecto al número de ufc inoculadas, en concreto 51-57%. Tras 24-72h a 35ºC aprox, turbidez de ligera a elevada.
- Pluralibater gergoviae MKTD 9245*, Excelente: Tras 20-30 minutos a 20-30°C, resiembra en TSA y obtención de >50-150% de colonias respecto al número de ufc inoculadas, en concreto 95%. Tras 24-72h a 35ºC aprox, turbidez de ligera a elevada.
*Las colecciones TIPO prohiben el uso de su referencia, por lo que indicamos la nuestra, directamente trazable a la colección TIPO.
PRESENTACION:
MEDIO DESHIDRATADO, TUBOS Y FRASCOS PREPARADOS CON Y SIN PERLAS DE VIDRIO Y A DIFERENTES CONCENTRACIONES
NOTA: Medio altamente recomendado para solución madre, diluciones y preenriquecimiento en muestra cuyos componentes interfieran con la flora:
La composición del medio permite asegurar una buena dispersión del inóculo.
Emulsiona las grasas e inactiva los derivados de amonio cuaternario, (únicos conservantes que inactivan los medios clásicos con Lecitina yTween),
y provoca una total inactivación de los demás conservantes modernos que pueda llevar en su fórmula el cosmético, el alimento o la muestra,
incluidos parabenes e incluso Isotiazolinona,
además de Compuestos fenólicos: fenoxietanol, feniletanol, anilidos…,
Amonios cuaternarios, Surfactantes catiónicos, Aldehidos, Formaldehido, glutaraldehido, compuestos liberadores de formol,
Compuestos oxidantes, peróxidos, halógenos (Flúor, Cloro, Bromo, Iodo…), lejía,
Imidazoles, Clohexidina, Biguanida,
Sales metálicas (Cu, Zn, Hg), compuestos organomercuriales…
Además inactiva los metabolitos generados en su crecimiento por parte de los microorganismos acompañantes, que en otros caldos pueden impedir o enmascarar el crecimiento del organismo buscado.
CRÉDITOS
En un estudio intercolaborativo realizado para comparar todos los caldos generales, es el que más flora total recupera y el segundo (tras el BHI Broth) que más patógenos recupera (“Estudio comparativo entre los distintos caldos de cultivo generales”. SANCHIS, J. XI Congreso Nacional de Microbiología de Alimentos. Pamplona, 9/1998).
En los servicios intercompartivos SEILAPARFUM y SEILALIMENTOS demuestra ser el mejor medio inicial para todo (diluciones para recuentos y revitalización/pre-enriquecimiento para búsqueda de patógenos).
Medio validado mediante intercomparación (puede bajarse la validación actualizada de microbiología cosmética, de la web www.microkit.es, pestaña publicacionesy validaciones).
SIEMBRA E INTERPRETACIÓN
Sembrar 1-25 gramos de muestra en 10-225 ml de medio.
Agitar y dejar reposar-actuar 20-30 minutos a temperatura ambiente.
Para realizar recuentos, sembrar en los agares adecuados sin previo enriquecimiento.
Si se desea investigar patógenos, enriquecer incubando a 32-35 ºC, 36-48 horas (ni menos, ni más) y después estriar en la superficie de las placas de los agares adecuados.
El usuario final es el único responsable de la destrucción de los organismos que se hayan desarrollado, según la legislación medioambiental vigente. Autoclavar antes de desechar en la basura.
https://www.microkit.es/fichas/LPT-NEUTRALIZINGBROTH-INCOLORO.pdf
Si desea más información sobre nuestro LETHEEN LPT NEUTRALIZING BROTH INCOLORO póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16