CROMOKIT MAXIM TSA AGAR CROMOGÉNICO es un medio cromogénico general, dopado para recuperar el máximo posible de microorganismos
Recuento total con máxima recuperación en alimentos, aguas y cosméticos, basado en PCA (FIL,IDF,AOAC,APHA,ICMSF) y TSA (Farmacopea), que diferencia las colonias, incluso las más diminutas, de las partículas y del medio.
Recuperación superior (122%) al PCA y 116% respecto al TSA.
COMPOSICIÓN
Triptona 5,0 g
Peptona de soja 5,0 g
Extracto de levadura 2,5 g
Glucosa 1,0 g
Factores doping MICROKIT 5,0 g
Agar‑agar 10,5 g
Cromógeno c.s.
(Fórmula por litro)
pH final: 6,8 ± 0,2
PREPARACIÓN
Disolver 29 g de medio en 1 litro de agua destilada.
Calentar hasta ebullición, agitando para su completa disolución.
Repartir en tubos o frascos. Autoclavar a 121 ºC durante 15 min o preferiblemente a 116°C durante 15 minutos. No sobrecalentar ni mantener fundido mucho tiempo.
Refundir sólo una vez. El color final del medio es blanco-crema. A veces, por sobrecalentamiento, adquiere un tono rosado que retorna al crema cuando se vuelve a enfriar el medio, lo cual no afecta los resultados.
PARA USO EXCLUSIVO EN LABORATORIO.
MANTENGA EL BOTE BIEN CERRADO EN LUGAR SECO, FRESCO Y OSCURO.
AGITE EL BOTE ANTES DE USAR.
DESHIDRATADO CODIGO: BCD515
CONTROL DE CALIDAD DEL MEDIO CROMOKIT MAXIM-AGAR CROMOGÉNICO
Realizado en nuestro laboratorio; es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio, tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…).
DESHIDRATADO: Polvo grueso, Crema PREPARADO: Estéril, Crema
EVALUACIÓN DEL RENDIMIENTO ISO/TS 11133-2 24-48 h a 37 ºC o mejor 72 h a 30 ºC, aplicando el método ISO 4833, ISO 2293, o el indicado en el Manual MICROKIT: E. coli MKTA 25922, Excelente, colonias rojas, PR >70% en concreto 90-184 % * de colonias respecto al número de ufc certificadas e inoculadas en TSA.
Staphylococcus aureus MKTA 6538P, Excelente, colonias rojas, PR >70% en concreto 99-164 % * de colonias respecto al número de ufc certificadas e inoculadas en TSA. Bacillus subtilis MKTA 6633, Excelente, colonias rojas, PR >70% en concreto 99-129 % * de colonias respecto al número de ufc certificadas e inoculadas en TSA.
Micrococcus luteus MKTA 9341, Excelente, Colonias rojas en 48 h, crecen mucho más rápido y mejor que en TSA, y mejor a temperatura ambiente.
Enterococcus faecalis MKTA 29212, Excelente, colonias rojas, PR >70% en concreto 99-191 % *de colonias respecto al número de ufc certificadas e inoculadas en TSA.
Pseudomonas aeruginosa MKTA 9027, Excelente, colonias rojas.
* Esta variabilidad de la productividad depende de la composición y carga de la flora acompañante inoculada. Las colecciones TIPO prohiben el uso de su referencia por lo que indicamos la nuestra, directamente trazable a la colección TIPO.
PRESENTACIÓN
TUBOS 20 ml, FRASCOS 100 ml, MEDIO DESHIDRATADO.
Recuento total standard de bacterias aerobias en alimentos, aguas, productos farmacéuticos, cosméticos y otros productos.
Las colonias crecen en distintos tonos del rojo: rosa, naranja, purpura…. sobre el tono crema del medio (excepto ciertos acidolácticos y ciertas levaduras, que crecen con colonias blancas, sin viraje, por lo que este medio los distingue de los aerobios).
El color de las colonias no afecta a las pruebas de identificación posteriores que quisiera realizar.
MODO DE EMPLEO E INTERPRETACIÓN DE RESULTADOS
Inocular 1 ml de muestra y su serie de diluciones decimales, en masa.
Incubar a 30 ºC aproximadamente durante 48 horas. Con flora psicotrofa, incubar a 6 ºC aproximadamente durante 10 días y con flora termófila, incubar a 55 ºC aproximadamente durante 48 horas.
Contar todas las colonias. La recuperación supera el 20% por encima de la obtenida en PCA y el 16% por encima de la obtenida en TSA, gracias a ciertos factores doping de aerobios descubiertos y agregados por MICROKIT.
Esta fórmula, con menos agar, aumenta la sensibilidad del medio frente a los aerobios más lábiles, al permitir una mejor oxigenación del fondo.
Este medio está diseñado para siembra en masa. Si desea sembrar en superficie, añada 3-5 g/l de Agar-Agar (BCB006), o utilice 30-32 g/l de este mismo medio.
Para minimizar la desecación en muestreos de aire y superficies, o para siembra en Spiral, añadir 2 gotas de antiburbujas (SBL001) por cada litro de agua, antes de añadir el medio y antes de autoclavar.
Para contar por separado las bacterias, de las levaduras y mohos, añadir a un duplicado, enfriado a 45°C, 0,05-0,5 g/l de Cicloheximida (SKM200): En la placa con CEX sólo crecerán las bacterias y en la placa sin CEX , la suma de bacterias + levaduras y mohos.
El usuario es el único responsable de la eliminación de los microorganismos según la legislación medioambiental vigente. Autoclavar antes de desechar a la basura.
Si desea más información sobre nuestro CROMOKIT MAXIM-AGAR CROMOGÉNICO o cualquier otro producto no dude en contactar con nosotros a través de nuestro correo electrónico microkit@microkit.es.
Haga sus pedidos en pedidos@miccrokit.es
https://www.microkit.es/fichas/CROMOKIT-MAXIM-AGAR-CROMOGENICO.pdf
Prepárese para más de una sorpresa informativa cuando vea nuestro video sobre los medios Cromogénicos: https://www.youtube.com/watch?v=-JVPVWxY8ZE&t=271s

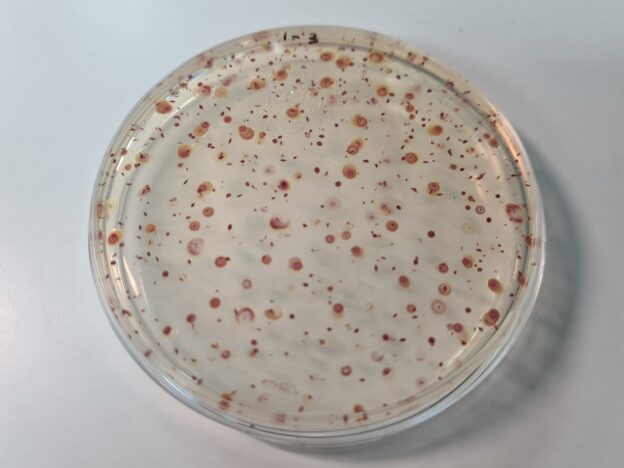





 y a causa de no ser metabolizado por las bacterias, el Agar-Agar es el soporte universal para aislamiento de microorganismos en microbiología.
y a causa de no ser metabolizado por las bacterias, el Agar-Agar es el soporte universal para aislamiento de microorganismos en microbiología.






 Sembrar en superficie 0,1 ml de muestra o una membrana filtrada. Incubar durante 3-21 días a temperatura primaveral (aproximadamente 21-28°C) a la luz indirecta del sol, con fotoperiodo de aproximadamente 16 horas de luz, 8 horas de oscuridad (si no es primavera o el laboratorio está en zona poco clara, ayudar con fluorescentes para acercarse lo más posible al fotoperiodo mencionado, clave de más rápidos resultados). El usuario es el único responsable de la eliminación de los microorganismos según la legislación medioambiental vigente. Autoclavar antes de desechar a la basura.
Sembrar en superficie 0,1 ml de muestra o una membrana filtrada. Incubar durante 3-21 días a temperatura primaveral (aproximadamente 21-28°C) a la luz indirecta del sol, con fotoperiodo de aproximadamente 16 horas de luz, 8 horas de oscuridad (si no es primavera o el laboratorio está en zona poco clara, ayudar con fluorescentes para acercarse lo más posible al fotoperiodo mencionado, clave de más rápidos resultados). El usuario es el único responsable de la eliminación de los microorganismos según la legislación medioambiental vigente. Autoclavar antes de desechar a la basura.