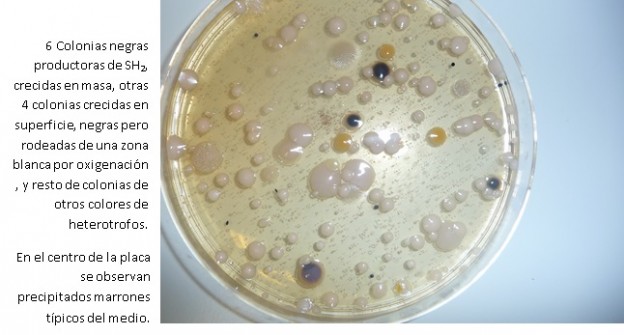
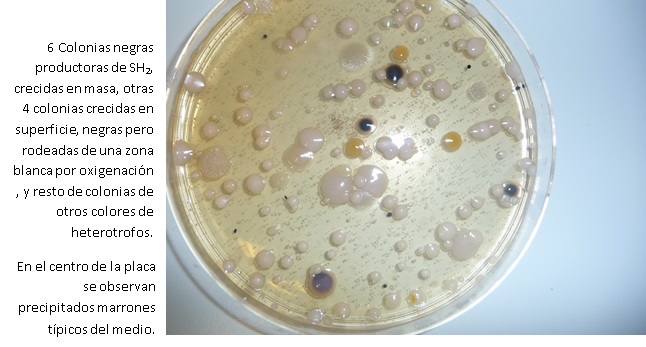
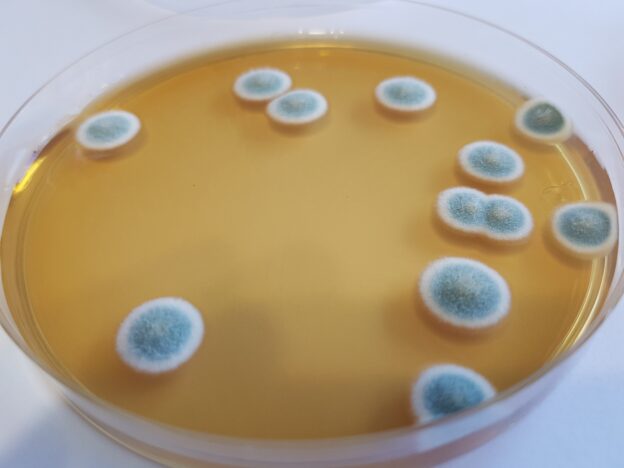
LISTERIA TSB-YE AGAR es el Agar ISO para aislar colonias de Listeria previo a su confirmación bioquímica (ej: con Xilosa/Rhamnosa MICROKIT) .
Agar para selección de colonias de Listeria y su confirmación (ISO 11290-1:1997, 11290-2:2000)
COMPOSICIÓN
- Triptona de caseína 17.00 g
- Peptona de soja 3.00 g
- Cloruro sódico 5.00 g
- Fosfato dipotásico 2.50 g
- Glucosa 2.50 g
- Extracto de Levadura 6.00 g
- Agar-Agar 15.00 g
(Fórmula por litro)
pH final: 7.3 ± 0.2
PREPARACIÓN
Disolver 51 g de medio en 1 l de agua bidestilada, volteando varias veces hasta su total homogeneización. Autoclavar a 121 ºC durante 15 minutos. El color final del medio es crema.
PARA USO EXCLUSIVO EN LABORATORIO
MANTENGA EL BOTE BIEN CERRADO EN LUGAR SECO, FRESCO Y OSCURO. AGITE EL BOTE ANTES DE USAR
DESHIDRATADO CODIGO: DMT156
CONTROL DE CALIDAD DEL MEDIO
Realizado en nuestro laboratorio; es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio, tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…)
DESHIDRATADO: polvo crema
PREPARADO: crema
EVALUACIÓN DEL RENDIMIENTO ISO/TS 11133-2 24 h a 37 ºC Aplicando el método ISO 11290 o el indicado en el Manual MICROKIT actualizado:
- Listeria monocytogenes.MKTA 7644, Buen crecimiento
Las colecciones TIPO prohiben el uso de su referencia por lo que indicamos la nuestra, directamente trazable a la colección TIPO.
PRESENTACIÓN: MEDIO DESHIDRATADO
MODO DE EMPLEO E INTERPRETACIÓN DE RESULTADOS
Inocular con una colonia aislada. Incubar a 35 ºC ó 37 ºC aproximadamente, 18-24 h o hasta que el crecimiento sea satisfactorio. Partir de este cultivo para realizar pruebas bioquímicas e inmunológicas.
https://www.microkit.es/fichas/LISTERIA-TSB-YE-AGAR.pdf
El usuario final es el único responsable de eliminar los microorganismos de acuerdo con la legislación medioambiental vigente. Autoclavar antes de desechar a la basura.
Si desea más información sobre nuestros LISTERIA TSB-YE AGAR rellene nuestro formulario de contacto http://www.medioscultivo.com/contacto . O si lo prefiere póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16
https://www.microkit.es/monograficos/3-Listeria-monocytogenes-monograf–a.pdf