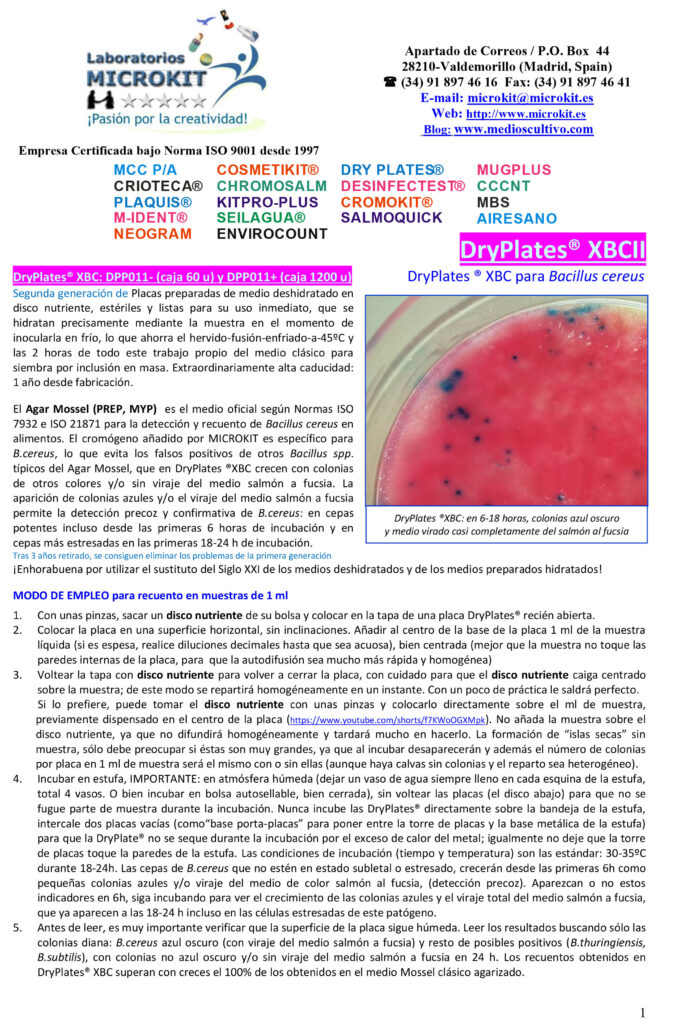
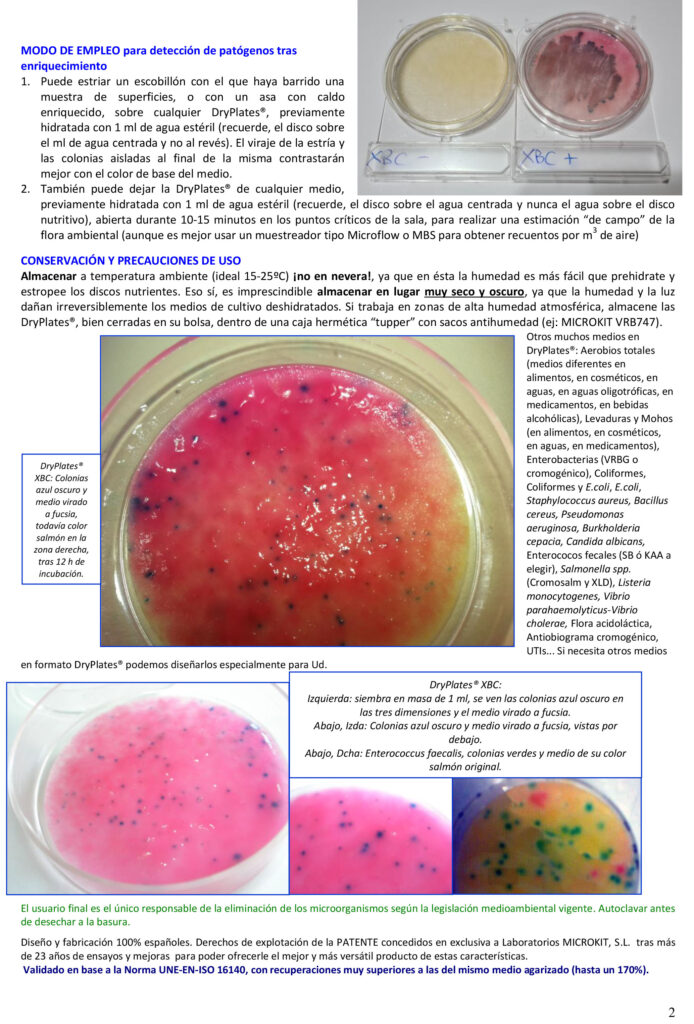
Prevención de la Hinchazón Tardía del Queso: Presentamos BUTYRIKIT
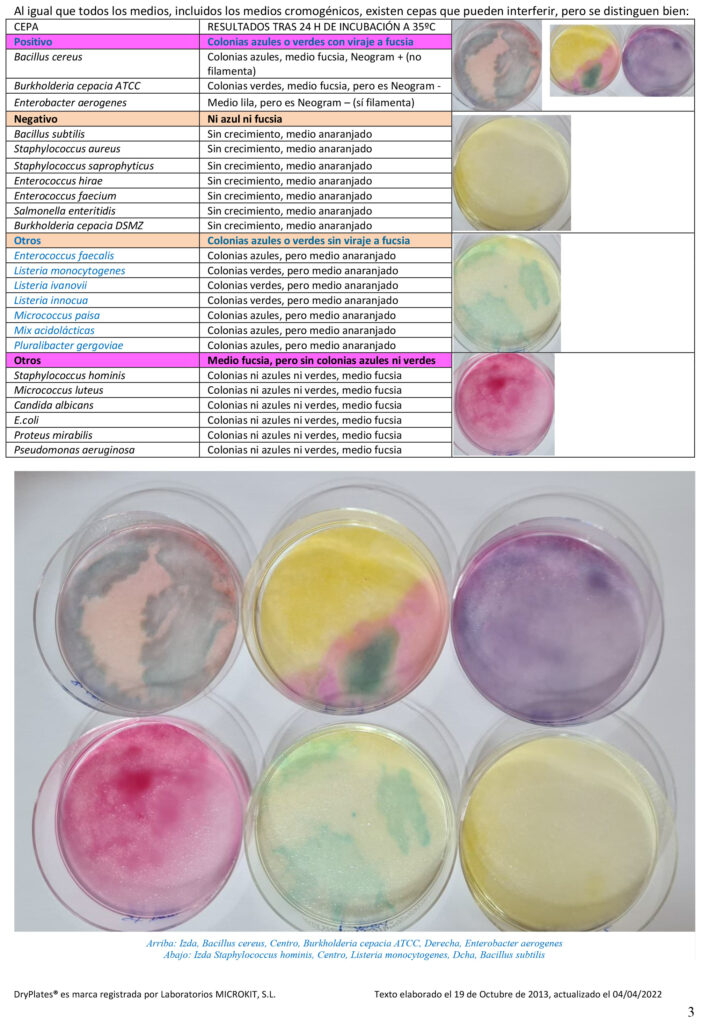
La hinchazón tardía es una preocupación que afecta, en algún momento, a casi toda la industria quesera, especialmente en épocas de sequía. BUTYRIKIT ofrece tubos listos para usar con el medio Bryant-Burkey, la herramienta esencial para detectar a tiempo el microorganismo causante de este problema y proteger su producción.
El Problema: Clostridium tyrobutyricum
Este microorganismo es un huésped común en el suelo seco y los ensilados. Las vacas, cabras u ovejas pueden ingerirlo al pastar, y de ahí pasa directamente a la leche. Una vez en el queso, se multiplica de manera lenta pero implacable.
- El Riesgo: La bacteria genera gases durante su metabolismo, produciendo grietas y estropeando la textura del queso. Lo más preocupante es que basta con una sola célula de este microorganismo en 10 ml de leche para que, a largo plazo, toda la pieza se arruine.
- La Consecuencia: Si la hinchazón tardía no se previene, cuando se detecta, suele ser demasiado tarde. La partida completa de queso curado ya se habrá resquebrajado, resultando en pérdidas significativas.
Solución Rápida y Fiable con BUTYRIKIT
Para la industria quesera, es de vital importancia preventiva analizar la ausencia de este patógeno en una muestra de 10 ml de leche. Si el análisis resulta positivo, se está a tiempo de actuar añadiendo clorhidrato de lisozima u otros aditivos autorizados antes de que sea demasiado tarde.
Nuestros Tubos Preparados (Ref: TPL006) están diseñados para una máxima eficacia:
- Selectividad Avanzada: El medio Bryant-Burkey, junto con lactato de sodio, acetato de sodio y clorhidrato de cisteína, inhibe el crecimiento de otras bacterias, potenciando exclusivamente el crecimiento de Clostridium tyrobutyricum.
- Detección de Oxígeno (Resazurina): La resazurina incorporada actúa como un indicador de seguridad. Si el medio se torna rosado, detecta un aumento del oxígeno, que sería letal para el Clostridium. Esto asegura que las condiciones de prueba sean óptimas.
- Facilidad de Uso: La parafina ya está incorporada en el tubo, simplificando enormemente el proceso para el analista. También ofrecemos tubos sin parafina si prefiere añadirla Ud. tras añadir la muestra
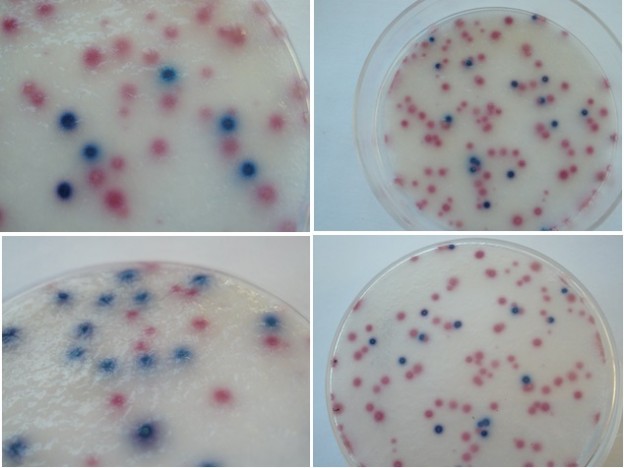
Cómo Interpretar el Resultado (Criterio de Positivo):
- Un resultado es positivo si observa un desarrollo gaseoso en el tubo que levante el tapón de parafina.
Garantía de Negativo:
- Dado que una sola célula en 10 ml de leche puede causar la enfermedad, si su cultivo resulta negativo, usted tendrá la tranquilidad de que su queso no sufrirá la temida hinchazón tardía.
Mención Adicional: Hinchazón Maloliente
También existe un problema similar, aunque más raro, la hinchazón maloliente del queso, causada por Clostridium sporogenes. Este microorganismo es proteolítico y produce el desagradable sulfuro de hidrógeno. Para la detección de Cl. sporogenes, recomendamos los tubos preparados de Agar parafinado SPS TPL049 de LABORATORIOS MICROKIT.
Para obtener más información sobre nuestros medios de cultivo y kits, así como precios actualizados, no dude en ponerse en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16.
https://www.microkit.es/fichas/BRYANT-BURKEY-TYROBUTYRICUM-BROTH.pdf