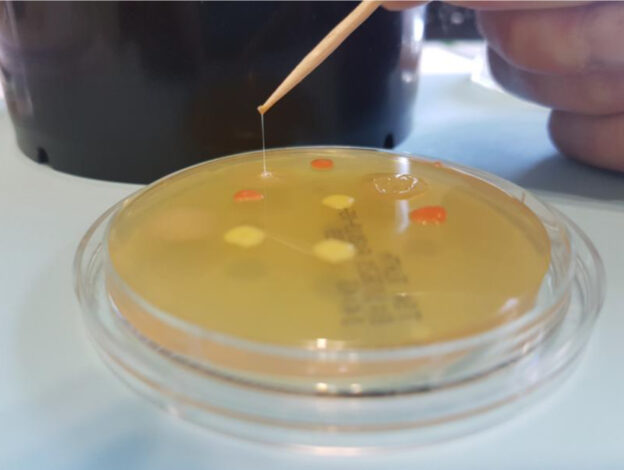
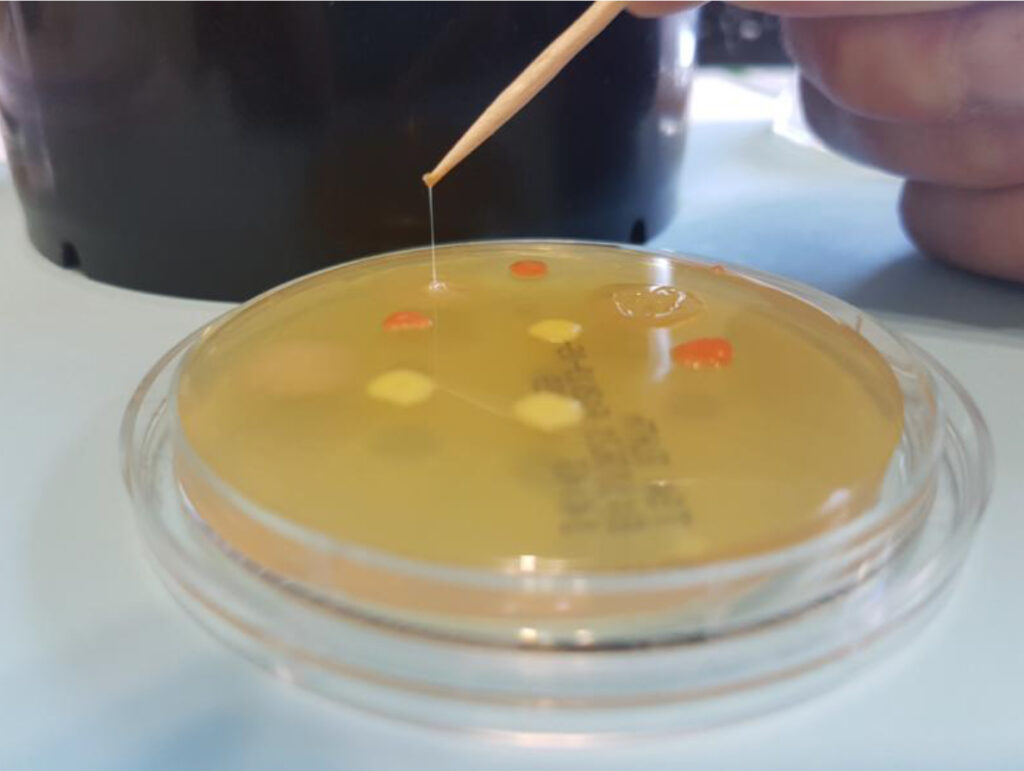
ENTEROCULT P/A BOTE 100 g ESTÉRIL
detección económica enterococos aguas: Con los botes de 100 g de Enterocult podrá buscar enterococos en aguas por sólo 1 €
El método P/A
(Presencia/Ausencia) fue inventado durante la segunda guerra mundial para evitar que los soldados murieran por beber aguas contaminadas. Desde la década de los 1990, MICROKIT ha ido desarrollando numerosos Kits P/A cromogénicos para control de patógenos en aguas. Estos kits no sólo triunfan en todo el mundo gracias a las ONG que trabajan en la mejora del agua de bebida de los países tropicales, sino que además están reconocidos como el método más fiable, de acuerdo con sus numerosas validaciones y participaciones en servicios intercomparativos. Se pueden emplear en trabajo de campo y en el laboratorio y ahorran tanto el trabajo de filtración de membrana (MF) o de NMP, como su coste. Con ellos se puede decir
¡de la muestra a la estufa en 10 segundos!
En el caso de las aguas y muestras líquidas incoloras, simplemente se agrega a los 100 (ó 250 ml) de muestra de agua el medio estéril adecuado para el microorganismo que se busca; se incuba; y al día siguiente, si no ha cambiado de color, se demuestra la ausencia del patógeno (sin falsos negativos) y si ha cambiado al color indicado, se demuestra su presencia. Así de sencillo. Y más efectivo que ningún otro método. Porque el método P/A no estresa los microorganismos como sucede con la MF, que obtiene recuperaciones muy deficientes.
La legislación europea exige el recuento de E.coli (y demás coliformes), Enterococos fecales y Clostridium perfringens y sus esporas en aguas de consumo humano para demostrar que no hay ni una sola célula en 100 mL; y en aguas envasadas, el recuento de E.coli (y demás coliformes), Enterococos fecales, Clostridium sulfito reductores y Pseudomonas aeruginosa para demostrar que no hay ni una sola célula en 250 mL. Dado que más del 99,99% de las muestras que Ud. analiza, están exentas de estos microorganismos,
está gastando enormes cantidades de tiempo y de dinero en “contar ceros”.
Cambie al método P/A y todas las ausencias las debe informar como “cero”, ya que no existen células decimales, por lo que en microbiología, ausencia es exactamente lo mismo que cero. Y cuando tenga alguna presencia, repita el análisis por MF e informe del recuento que obtenga. De este modo tan sencillo de “screening negativo”, va a ahorrar ingentes cantidades de tiempo y de dinero, pero además, va a aumentar la fiabilidad de sus análisis, ya que
el método P/A detecta numerosas presencias que el método MF encuentra como “cero”,
que son los peligrosos falsos negativos. ¡Se acepta en la bibliografía internacional que cerca del 6 % de las aguas que contienen Enterococos fecales, no son detectadas como positivas mediante el método MF!
Hasta ahora la presentación del método P/A MICROKIT era en frascos estériles con medio líquido para agregar dentro 100 ml de muestra de agua (referencias RPL3..). O bien la versión económica en viales de medio en polvo estéril para añadir un vial a 100 ml de muestra de agua (no incluido el bote estéril, referencias FPA9..). Por petición de nuestros mayores usuarios, extendemos desde finales de 2016 su uso en una
nueva presentación extraordinariamente económica: Botes de 100 g de polvo estéril con cucharilla esterilizable
(referencias DMTI9..-).
En esta nueva presentación, que le llega estéril, debe abrir el bote cada vez que lo use, en cabina o junto a un Bunsen, extraer con la cucharilla esterilizada (o sumergida en alcohol y tras dejar que se seque) el volumen indicado de medio, y cerrar el bote inmediatamente para evitar que se contamine. A pesar de que es difícil que esto suceda, ya que ninguno de los microorganismos implicados habitan en el aire. Use guantes estériles al manipularlo, para no contaminar el resto del polvo interior de eventuales células de Enterococos fecales que pudiera portar en sus manos.
MODO DE EMPLEO
1-Añada una cucharadita (1 gramo) de P/A ENTEROCULT para buscar Enterococos fecales en 100 ml de agua (dos cucharaditas para buscarlos en 250 ml de agua). No hace falta enrasar ni ser muy estricto en el volumen de medio añadido, ya que el medio funciona perfectamente incluso a la mitad y al doble de la concentración indicada. Si el agua es clorada, añadir el tiosulfato sódico correspondiente para neutralizarlo.
2-Agitar, incubar a 37ºC
LECTURA DE RESULTADOS
3-Ver al día siguiente si hay cambio de color ámbar a negro-opaco (presunto positivo de Enterococo fecal) o no (negativo confirmado de Enterococo fecal).
4-En caso positivo hacer pruebas de confirmación adecuadas (cocos en cadenas, catalasa negativos). En caso negativo declarar la muestra como ausente de estos patógenos/indicadores en 100 (ó 250 mL) de muestra de agua.
PRESENTACIÓN
Bote de polvo estéril 100g y cucharilla para Enterococos fecales, Ref: DMTI901- para 50-100 muestras, con ¡3 años de caducidad!
detección económica enterococos aguas: Con los botes de 100 g de Enterocult podrá buscar enterococos en aguas por sólo 1 €
https://www.microkit.es/fichas/P-A-ENTEROCULT-BOTE-100g-esteril.pdf
El usuario final es el único responsable de la destrucción de los organismos que se hayan desarrollado, según la legislación medioambiental vigente.
Si desea más información sobre nuestros KIT P/A ENTEROCULT BOTE 100 g ESTÉRIL rellene nuestro formulario de contacto http://www.medioscultivo.com/contacto . O si lo prefiere póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16
No se pierda nuestro vídeo de los viales P/A:














 ya se emplean de rutina miles de unidades en todo el mundo.
ya se emplean de rutina miles de unidades en todo el mundo. anual es necesaria en cualquier caso y más frecuentemente cuantos más muestreos se realicen. Las fábricas con varias plantas pueden tener un MBS por planta y un solo KIT de validación para todas ellas. También deben exigir que el importador tenga un KIT de calibración para poder externalizar las calibraciones y no tener que comprar el KIT de calibración.
anual es necesaria en cualquier caso y más frecuentemente cuantos más muestreos se realicen. Las fábricas con varias plantas pueden tener un MBS por planta y un solo KIT de validación para todas ellas. También deben exigir que el importador tenga un KIT de calibración para poder externalizar las calibraciones y no tener que comprar el KIT de calibración.