CLOSTRICULT P/A DETECCIÓN VALIDADA POR MICROKIT Y POR IELAB PARA DETECCIÓN CERTERA DE CLOSTRIDIUM PERFRINGENS EN AGUA
CLOSTRICULT P/A DETECCIÓN VALIDADA
Detección Presencia / Ausencia (P/A) de Clostridium perfringens y sus esporas en 100 ml de agua
https://www.microkit.es/fichas/P-A-CLOSTRICULT-UE2-2019.pdf
INTRODUCCIÓN:
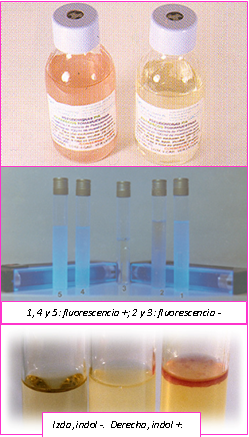
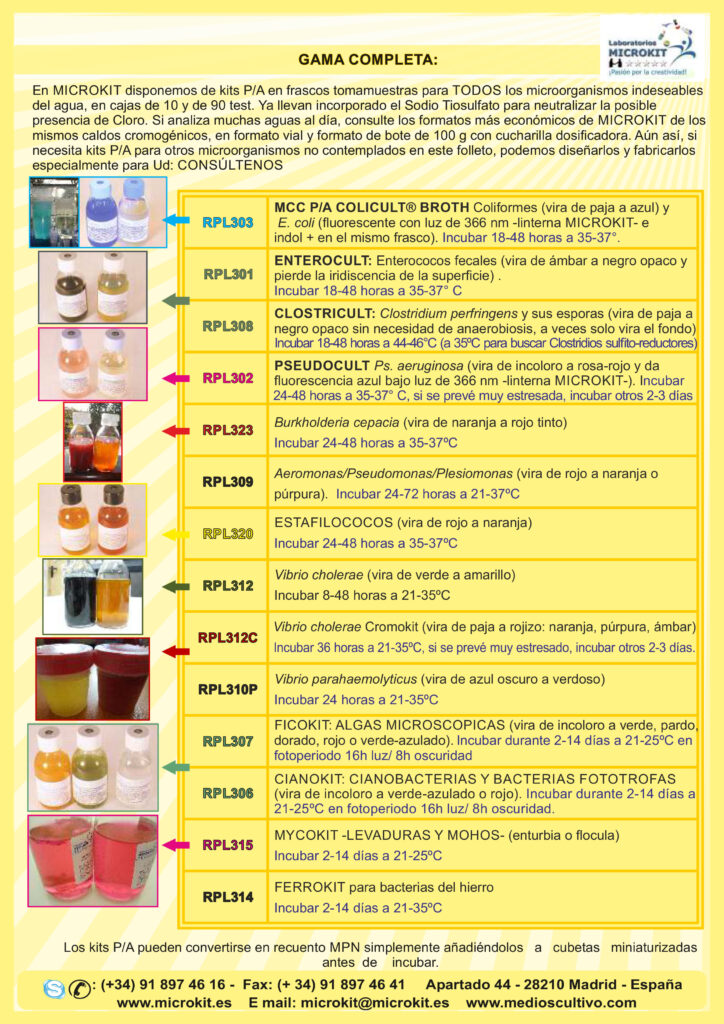
Medio estéril CLOSTRICULT Cromogénico diseñado por MICROKIT con base TSC y atmósfera de anaerobiosis para detección P/A (o recuento en su formato Quanti-P/A Ref: QPA-CP) de C.perfringens y sus esporas (el agua vira a negro opaco), que puede elegir en tres formatos diferentes:
- RPL308 Frascos tomamuestras con caldo estéril hidratado y tapón a rosca para añadir en ellos 100 mL de la muestra de agua. Cajas 10u ó 9x10u

- FPA902 Viales prepesados de polvo estéril con tapón a rosca para añadir a 100 mL de la muestra de agua (no incluido bote 100 mL VML155 o bolsa standup 100 mL B2787B estériles). Cajas 40u ó 10x40u

- DMTI902- Botes 100 g de polvo estéril y cucharilla dosificadora paraañadir a 100 mL de la muestra de agua (no incluido bote 100 mL VML155 o bolsa standup 100 mL B2787B estériles), Bote para 33 test

De gran utilidad como screening negativo de muestras rutinarias, al ser un método más fácil de emplear que la filtración de membrana y más fiable (escasez de falsos positivos y de falsos negativos, que en filtración de membrana es de nada menos que el 21% de las muestras analizadas en el mundo, por el estrés provocado durante la filtración).
También muy útil para que las potabilizadoras no dejen de analizar en festivos y fines de semana, ya que este método puede ser empleado por personal no especialista en microbiología, el mismo guarda de la depuradora puede hacerlo. La única precaución es que el operario no toque ni el agua ni el polvo con sus manos, para evitar contaminaciones artificiales.
Recuerde que este parámetro es el único indicador de probable presencia de Enterovirus-Norovirus y protozoos (Cryptosporidium, Giardia, Entamoeba…) en el agua.
MODO DE EMPLEO:
Es necesario tratar previamente el agua clorada, mediante Tiosulfato Sódico, para que las células dañadas subletalmente se recuperen, excepto en los frascos tomamuestras RPL308, que ya lo incluyen.
Añadir los 100 mL de agua de muestra en el frasco o en el recipiente estéril que se va a utilizar; en el caso de los viales, añadir todo el contenido sobre el agua; en el caso de los botes de 100g, añadir tres cucharaditas rasas sobre el agua y cerrar el bote con la cucharilla dentro para los posteriores usos. Voltear sin agitar para homogeneizar sin oxigenar. Incubar 18-48 horas a 35-37° C (según nuestras recomendaciones) ó a 42° C (según Normas ISO).
Si desea detectar sólo esporas, provocar un shock térmico: calentar la muestra de 100 ml de agua 15 minutos a 70-80 ºC antes de añadir el medio. No es necesario incubar con atmósfera de anaerobiosis, ya que el medio ya la incorpora. La muestra inoculada sirve también de medio de transporte, por lo que no es necesario incubar inmediatamente después de la toma de la muestra, pudiendo transcurrir varias horas entre toma e incubación.
Para aguas envasadas o de baño, se analizan 50 mL, por lo que debe añadir 50 mL de agua estéril a los 50mL de agua de muestra, o bien emplear el medio a la mitad de la concentración indicada.
INTERPRETACIÓN DE RESULTADOS:
El viraje a color negro-opaco (aunque sólo sea en el fondo, que es por donde suele empezar a virar) demuestra la Presencia de Clostridium perfringens y sus esporas en la muestra de agua.
Es necesaria la ausencia (no viraje), que equivale a 0 ufc/100 mL (ó en 50 mL). Sólo en caso positivo debería repetirse la muestra por método cuantitativo si se requiere un recuento concreto, aunque la legislación exige 0 y por tanto no importa si hay 2 ó 950, en ambos casos el agua no es potable. Si aún asi debe cuantificar(muestras positivas con Clostricult P/A), utilice Quanti-P/A-TSC (Ref: QPA-CP), que contienen este mismo medio con gelificantes en frío y atmósfera de anaerobiosis en una bolsa hermética.
Material necesario no incluído:
Tiosulfato Sódico para eliminar el cloro (SMT976) excepto en los frascos tomamuestras RPL308, que ya lo incluyen. Bote estéril 100ml (VML155), o bolsa estéril autosellable Stand-Up (B2787B). Estufa o incubador 35-37ºC (SIL12AR ó SIL24AR).
En homenaje a nuestro querido amigo, el Dr. Juan José Marcén, que falleció antes de conocer el éxito mundial de la fantástica idea que nos regaló en los años 90, el kit de coliformes/E.coli se regala a todas las ONGs que nos los pidan junto con otros parámetros P/A.
PARA USO EXCLUSIVO EN LABORATORIO O PARA ANÁLISIS DE CAMPO. MANTENER FUERA DEL ALCANCE Y DE LA VISTA DE LOS NIÑOS Y ANIMALES.
EXTREMADAMENTE HIGROSCÓPICO: MANTENGA EL BOTE BIEN CERRADO EN LUGAR SECO, FRESCO Y OSCURO. AGITE EL BOTE ANTES DE USAR. EN ZONAS DE ELEVADA HUMEDAD AMBIENTAL, GUARDAR EL BOTE BIEN CERRADO EN UN TUPPER HERMÉTICO CON SILICAGEL.
CONTROL DE CALIDAD:
Realizado en nuestro laboratorio; es prudente repetirlo en su laboratorio siempre que varíen las condiciones (más de 3 meses sin usar, tras desinfectar laboratorio, tras largos fletes, tras conservar a alta Tª, cuando adquiere aspectos extraños aunque no haya llegado la fecha de caducidad teórica de la etiqueta,…)
DESHIDRATADO: Polvo crema PREPARADO: Crema
CONTROL DE CRECIMIENTO 18-48 h a 37°C aproximadamente:
- Clostridium perfringens WDCM 00007, vira a negro opaco desde las primeras 18h si el inóculo es elevado y no procede de muestras estresantes, en 48h en caso contrario.
- E.coli WDCM 000013: Inhibido
- Pseudomonas aeruginosa WDCM 00026: Inhibido.
- Enterococcus faecalis WDCM 00009: Inhibido.
Para recuento NMP
este kit no se puede emplear con cubetas miniaturizadas, ya que la anaerobiosis quedaría comprometida. Por eso inventamos Quanti-P/A Clostricult: https://www.microkit.es/pdf/Quanti-PA-Clostricult-FOTOS2018.pdf
El usuario es el único responsable de la eliminación de los microorganismos según la legislación medioambiental vigente. Autoclavar antes de desechar a la basura.
Si desea más información sobre nuestro MICROKIT® P/A CLOSTRICULT rellene nuestro formulario de contacto http://www.medioscultivo.com/contacto . O si lo prefiere póngase en contacto con nosotros a través de nuestro correo electrónico microkit@microkit.es o por teléfono en el nº 91-897 46 16
No se pierda nuestro vídeo de los viales P/A: